🤖 Краткий пересказ от ИИ
Данное ретроспективное исследование было направлено на изучение взаимосвязи между уровнем онкомаркера CA125, статусом мутации BRCA1/2 и менопаузой у женщин с высоким риском рака яичников. Анализ охватил данные 466 пациенток, чтобы получить больше информации о клинических факторах, влияющих на уровень CA125.
Результаты показали, что уровень CA125 значительно выше в пременопаузе, чем в постменопаузе, и снижается с возрастом как у носителей мутации BRCA, так и у женщин без нее. Важно отметить, что наследственные мутации BRCA1/2 сильнее влияют на это снижение, что может потребовать пересмотра пороговых значений CA125 для оптимизации скрининга, в том числе с использованием современных УЗИ аппаратов.
✅ Ключевые тезисы из статьи:
- Диагностика: Современный скрининг рака яичников у женщин высокого риска включает анализ CA125 и трансвагинальное УЗИ, но его эффективность ограничена.
- Лечение: Единственным доказанным методом снижения смертности для женщин с мутацией BRCA1/2 является риск-уменьшающая сальпингоофорэктомия (РУСО).
- Преимущества: Исследование представляет собой одну из крупнейших когорт по изучению уровня CA125 у носителей мутации BRCA1/2 с учетом менопаузального статуса.
- Ограничения: Ограничения исследования включают ретроспективный характер, определение менопаузы только по возрасту и невозможность учета всех факторов, влияющих на CA125.
Последнее обновление: 21 июля 2025 р.
Экспертная проверка: Материал проверен и отредактирован экспертами RH.ua
Примечание об ИИ: Этот блок создан с помощью генеративного ИИ для быстрого ознакомления с основными идеями статьи. Для полного понимания темы рекомендуем прочесть полный текст.
⚠️ Не заменяет медицинскую консультацию
Резюме
Предусловия
Скрининг рака яичников у носителей мутации BRCA1/2 включает определение углеводного антигена 125 (CA125) и трансвагинальное ультразвуковое исследование (ТВУ), несмотря на низкую чувствительность и специфичность. Мы оценили связь между уровнем СА125, статусом мутации BRCA1/2 и менопаузой, чтобы предоставить больше информации о клинических состояниях, которые могут влиять на уровень СА125.
Методы
Мы ретроспективно проанализировали повторные измерения уровня СА125 и клинические данные 466 женщин с высоким риском развития рака яичников. Уровни СА125 сравнивали между женщинами с и без вредных мутаций в BRCA1/2. Для определения связи между возрастом и уровнем СА125 в сыворотке крови использовали корреляцию Пирсона. Различия в уровнях СА125 оценивали с помощью U-критерия Манна-Уитни. Влияние мутационного статуса BRCA1/2 и менопаузального статуса на изменение уровня СА125 определяли с помощью двухфакторного дисперсионного анализа (ANOVA).
Результаты
Уровень СА125 в сыворотке крови женщин в пременопаузе (медиана 13,8 кОд/мл; диапазон 9,4-19,5 кОд/мл) был значительно выше, чем у женщин в постменопаузе (медиана 10,4 кОд/мл; диапазон 7,7-14,0 кОд/мл; p < .001). Не было выявлено достоверной разницы в уровнях СА125 у носителей и не носителей мутации BRCA во всех возрастных группах (p = 0,612). При исследовании комбинированного влияния мутации BRCA1/2 и менопаузального статуса дисперсионный анализ выявил значительное взаимодействие между статусом мутации BRCA1/2 и менопаузальным статусом на уровне CA125 (p < 0,001). Наблюдалась значительная разница между уровнями СА125 у женщин в пременопаузе и постменопаузе, с большим эффектом у носителей мутации BRCA (p < 0,001, d = 1,05), тогда как у носителей без мутации наблюдался лишь небольшой эффект (p < 0,001, d = 0,32).
Заключение
Наши результаты свидетельствуют о том, что наследственные мутации в BRCA1/2 влияют на снижение уровня СА125 с возрастом. Чтобы доказать однозначное влияние этой мутации на уровень СА125, необходимо провести проспективные исследования, чтобы определить новые уровни отсечения СА125 у носителей мутации и оптимизировать скрининг рака яичников.
Предусловия
Эпителиальный рак яичников является наиболее летальным гинекологическим раком с общей выживаемостью 46% после установления диагноза. Неблагоприятный прогноз главным образом обусловлен обычно запущенной стадией заболевания на момент установления диагноза из-за бессимптомного течения рака яичников (РЯ) [1]. Женщины, которые относятся к группе “высокого риска” развития рака яичников, как правило, имеют отягощенный семейный анамнез по раку яичников, а также раку молочной железы и являются носителями патогенных мутаций в генах, которые подавляют онкогенез этих заболеваний. Мутации зародышевой линии в генах BRCA1 и BRCA2 ассоциируются с высоким риском развития РЯ и являются причиной около 15-20% всех случаев. Кумулятивный риск развития рака до 80 лет составляет 44% у носителей мутации BRCA1 и 17% у носителей мутации BRCA2 [2].
Для женщин с высоким риском мутаций BRCA1/2 риск-уменьшающая сальпингоофорэктомия (РУСО) является единственным доказанным вмешательством, снижающим смертность, для профилактики рака маточных труб и выявления скрытой неоплазии. Ее рекомендуют женщинам старше 35 лет, которые уже завершили детородный период [3, 4]. Хотя РУСО является очень эффективной, когда ее проводят в пременопаузе [4], она вызывает бесплодие и преждевременную менопаузу [5], что ассоциируется с повышенным риском развития остеопороза [6], а также сердечно-сосудистых [7] и неврологических заболеваний [8]. Некоторые женщины-носители мутации BRCA откладывают РУСО до менопаузы или вообще отказываются от вмешательства, несмотря на риски. Эти женщины особенно выиграют от эффективной стратегии скрининга РЯ [9, 10].
Современный скрининг для женщин с высоким риском включает определение онкомаркеров в сыворотке крови CA125 и трансвагинальное ультразвуковое исследование (ТВУ) каждые 6 месяцев [11]. Однако эффективность этих тестов является низкой, поскольку чувствительность и специфичность СА125 и ТВУ недостаточна для скрининга [12,13,14]. Измерение СА125 для ранней диагностики РЯ ограничено ложноотрицательными результатами из-за низкой чувствительности на ранних стадиях заболевания, а также ложноположительными результатами, возникающими из-за его повышения в физиологических и доброкачественных состояниях [15, 16]. К ним относятся гинекологические заболевания, такие как эндометриоз, а также негинекологические расстройства, такие как заболевания печени или панкреатит [17,18,19,20]. Демографические и клинические факторы, такие как раса, возраст и прием оральных контрацептивов, также влияют на уровень СА125 в сыворотке крови [21,22,23].
Уровень СА125 в сыворотке крови связан с функцией яичников и снижается с возрастом [16, 21], что приводит к значительно более высоким значениям у женщин в пременопаузе, чем в постменопаузе [24, 25]. Поэтому для женщин в постменопаузе рекомендуется пороговое значение 35 кОд/мл, тогда как для женщин в пременопаузе используется пороговое значение 50 кОд/мл [22]. Хотя современная диагностика РЯ базируется на наблюдении за уровнем СА125 выше указанных предельных значений, было показано, что повышение уровня со временем в пределах нормы также является признаком развития этого заболевания [10, 26, 27].
Связь между раком яичников и повышенным уровнем СА125 в сыворотке крови сильнее у женщин в постменопаузе, чем в пременопаузе [28]. Много исследований по серийным измерениям СА125 было проведено на женщинах в постменопаузе из популяций среднего риска [17, 21, 27, 29, 30]. Однако у большинства женщин с высоким наследственным риском рака яичников скрининг начинается до менопаузы [31]. Существующие схемы скрининга рака яичников не смогли обеспечить снижение смертности как в средней популяции, так и у пациенток с высоким риском [10, 12, 27]. Улучшение раннего выявления рака яичников является крайне необходимым, особенно для женщин с высоким наследственным риском.
Целью этого исследования было выяснить, существует ли разница в концентрации СА125 у женщин с мутацией в гене BRCA1 или BRCA2 и женщин без этой генетической мутации, а также проанализировать изменения концентрации в зависимости от возраста и менопаузального статуса.
Материалы и методы
Исследуемая популяция
Этот ретроспективный анализ базируется на данных женщин, участвовавших в программе раннего выявления наследственного рака молочной железы и яичников (НРМЯ) кафедры гинекологической онкологии Венского медицинского университета с 2000 по 2018 год. В эту когорту вошли женщины, которые считались имеющими повышенный риск развития рака молочной железы и яичников из-за отягощенной семейной истории и/или мутации в BRCA1/2. Мы сравнили данные женщин с вредной мутацией BRCA1/2 с данными женщин без вредной мутации BRCA1/2. Данные по уровню СА125 в сыворотке крови, статуса мутации BRCA1 или BRCA2, возраста, менопаузального статуса, РУСО и рака яичников были собраны путем ретроспективного анализа карт.
В исследовании участвовали женщины без рака яичников, которые прошли тестирование на мутации BRCA1 или BRCA2 и еще не прошли РУСО. Женщины с диагнозом рака яичников, неизвестным статусом мутаций BRCA1/2 или без измерения СА125 были исключены. Также были исключены женщины, в истории болезни которых было указано наличие эндометриоза или воспалительных заболеваний органов малого таза. Существовала значительная разница в количестве измерений СА125 на одну пациентку. Поэтому мы оценивали каждое измеренное значение СА125 как отдельный случай. Мы не смогли ретроспективно оценить большинство клинических факторов, которые могут существенно влиять на уровень СА125 у здоровых женщин. Это привело к значительному разнообразию значений СА125 в собранных нами данных, причем многие значения значительно превышали порог 35 кОд/л или 50 кОд/л. Клинические исследования, оценивавшие концентрацию СА125 в сыворотке крови у женщин с эндометриозом III/IV стадии, эндометриомой или воспалительными заболеваниями органов малого таза, преимущественно сообщали о средних уровнях СА125 в диапазоне от 60 до 70 кОд/л [32,33,34,35,36]. Исходя из этих данных, мы предположили, что в доброкачественных случаях со значениями СА125 более 70 кОд/л, наличие доброкачественного гинекологического заболевания является чрезвычайно высоким. Следовательно, мы исключили эти случаи из нашего анализа.
Учитывая наши критерии включения и исключения, мы смогли использовать в анализе данные 466 женщин с общим количеством 1305 измерений СА125. Популяционные исследования показали, что естественная менопауза обычно наступает в среднем в возрасте 51 года в странах с высоким уровнем дохода [37, 38]. Поэтому мы определили пациенток в возрасте ≥ 51 года и старше как постменопаузальных, у которых не было информации о менструальном анамнезе, за исключением случаев, когда была доступна конкретная информация из клинической карты о том, что пациентка все еще находилась в пременопаузе на момент скрининга. В противном случае женщины в возрасте < 51 года были классифицированы как женщины в пременопаузе. Характеристики пациенток приведены в таблицах 1 и 2.
Таблица 1 Характеристика женщин с высоким наследственным риском во время первого визита к врачу
| Мутация BRCA1/2 | В целом | ||
| Носителиa | Нет мутацииb | ||
| Возраст, лет | |||
| Среднее | 41 | 45 | 45,1 |
| Диапазон | 26—73 | 24—77 | 24—77 |
| Менопаузальный статус | |||
| Предменопаузальный период | 103 | 235 | 338 |
| % среди всех женщин в пременопаузе | 30,5% | 69,5% | |
| % от общего количества | 22,1% | 50,4% | 72,5% |
| В постменопаузе | 29 | 99 | 128 |
| % среди всех женщин в постменопаузе | 22,7% | 77,3% | |
| % от общего количества | 6,2% | 21,2% | 27,5% |
| Всего | 132 (28,3%) | 334 (71,7%) | 466 |
aНосители – женщины с вредной мутацией в генах BRCA1 или 2
bНет мутации – женщины без вредной мутации в генах BRCA1 или 2
Таблица 2 Распределение по возрасту и менопаузальному статусу женщин из группы высокого риска во время каждого измерения
| Мутация BRCA1/2 | В целом | ||
| Носителиa | Нет мутацииb | ||
| Возраст, лет | |||
| Среднее | 49 | 44 | 47,5 |
| Диапазон | 26—80 | 24—83 | 24 – 83 |
| Менопаузальный статус | |||
| Предменопаузальный период | 496 (38,1%) | 357 (27,4%) | 853 (65,4%) |
| Постменопаузальный период | 343 (26,2%) | 109 (8,3%) | 452 (34,6%) |
| Всего | 839 (64,3%) | 466 (35,7%) | 1305 (100%) |
aНосители – женщины с вредной мутацией в генах BRCA1 или 2
bНет мутации – женщины без вредной мутации в генах BRCA1 или 2
Статистический анализ
Статистический анализ проводили с помощью программы SPSS (IBM SPSS® 26.0). Сила связи между возрастом и уровнем СА125 в сыворотке крови определялась с помощью коэффициента корреляции Пирсона (r) при условии, что эти две переменные находятся в линейной связи. Дополнительно рассчитывали доверительные интервалы для коэффициента корреляции r методом бутстрапинга, оценивая истинное среднее значение выборки с вероятностью 95%. Бутстрапинг проводился путем повторной выборки случаев. Различия в уровнях СА-125 оценивали с помощью U-критерия Манна-Уитни. Влияние мутационного статуса BRCA1/2 и менопаузального статуса на изменение уровня СА125 определяли с помощью двухфакторного дисперсионного анализа (ANOVA). Для проверки однородности дисперсий использовали критерий Левенса. Для подтверждения наличия различий между группами проводили постфактум t-критерий Уэлча. Применялось двустороннее тестирование, р-значения ниже 0,05 считались статистически значимыми. Поправки на многократное тестирование не проводили, поскольку цели данного исследования являются исследовательскими. Для оценки степени различий результатов использовали размер эффекта d по Коэну, который предполагает, что d ≥ 0,20 является малым, d ≥ 0,50 – средним и d ≥ 0,80 – большим размером эффекта. Коэффициент корреляции r интерпретировался как размер эффекта для корреляции, при этом значение r ≥ 0,10 означает малый, r ≥ 0,30 – средний и r ≥ 0,50 – большой размер эффекта.
Результаты
Этот анализ базируется на данных 466 женщин, среди которых было проведено 1305 оценок концентрации СА125 в сыворотке крови (табл. 1 и 2). Средний возраст при первом визите составил 45,1 года (мин. 24,2, макс. 77,6) лет (табл. 1). Среднее количество измерений на одного пациента составляло 2,83 (СО = 3,33; мин. 1, макс. 38).
Уровни CA125 в зависимости от возраста
Независимо от мутационного статуса, наблюдается небольшая, но значимая отрицательная корреляция между возрастом и уровнем СА125 в сыворотке крови, r(1305) = -0,22; 95%-KI [-0,17; -0,28], p <0,001. Применяя соответствующее уравнение регрессии, Ŷ = 23,49 + (-0,182 * xi), можно предположить, что уровень СА125 в сыворотке крови 50-летней женщины измеряется на уровне 14,39 кОд/л, независимо от мутационного статуса. Учитывая мутационный статус, наблюдается очень небольшая, но значимая отрицательная корреляция между возрастом и уровнем СА125 в сыворотке крови, r(839) = -0,12; 95%-KI [-0,05; -0,19], p < 0,001, в случаях без мутации в BRCA1/2. Используя соответствующее корреляционное уравнение, Ŷ = 19,55 + (-0,104 * xi), можно предположить, что уровень СА125 в сыворотке крови 50-летнего носителя без мутации составляет 14,35 кОд/л. Для случаев с мутацией BRCA1/2 выявлена умеренная отрицательная корреляция, r(466) = -0,34; 95%-KI [-0,27; -0,42], p < 0,001. На основе соответствующего уравнения корреляции, Ŷ = 28,28 + (-0,288 * xi), можно предположить, что для 50-летнего носителя BRCA1/2-мутации уровень СА125 в сыворотке крови составляет 13,88 кОд/л.
Уровни CA125 у носителей мутации BRCA1/2 и носителей без мутации
Уровни СА125 были выше (p < 0,001) у женщин в пременопаузе (медиана 13,8 кОд/мл; диапазон от 9,4 до 19,5 кОд/мл), чем у женщин в постменопаузе (медиана 10,4 кОд/мл; диапазон от 7,7 до 14,0 кОд/мл). Уровни СА125 приведены в таблице 3.
Таблица 3 Уровни СА125 в сочетании с менопаузальным статусом, а также статусом мутации BRCA, проанализированные отдельно
| n | С ± СО | мин.-макс. | МД | ИКР | Средний ранг | |
| Менопаузальный статус | ||||||
| Пременопауза | 853 | 15.93 ± 9.32 | 2.70—67.70 | 13.9 | 9.5; 19.5 | 717.64 |
| Постменопауза | 452 | 12.11 ± 7.26 | 0.60—66.50 | 10.5 | 7.9; 14.0 | 531.02 |
| Всего | 1305 | 14.61 ± 8.85 | 0.60—67.70 | 12.0 | 8.8; 18.1 | |
| BRCA-мутационный статус | ||||||
| Отрицательнаяa | 839 | 14.31 ± 8.33 | 2.10 – 66.50 | 12.0 | 8.9; 17.7 | 649.05 |
| Положительнаяb | 466 | 15.16 ± 9.71 | 0.60 – 67.70 | 12.75 | 8.7; 18.8 | 660.11 |
| Всего | 1305 | 14.61 ± 8.86 | 0.60—67.70 | 12.0 | 8.8; 18.1 | |
Сокращение: n Количество, С Среднее значение, СО Стандартное отклонение, мин. Минимум, макс. Максимум, МД Медиана, ИКР Интерквартильный размах
aОтрицательный результат касается женщин без вредных мутаций в генах BRCA1 или 2
bПоложительные – женщины без вредной мутации в генах BRCA1 или 2
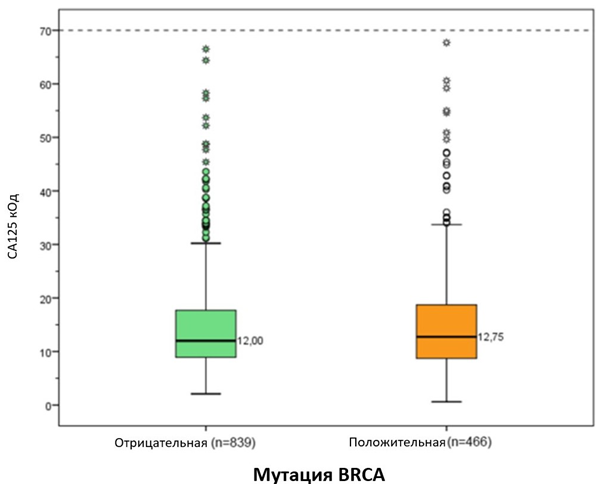
Мы не обнаружили достоверной разницы (p = 0,612) в уровнях СА125 у носителей мутации BRCA1/2 (медиана 12,75 кОд/мл; диапазон от 8,7 до 18,8 кОд/мл) по сравнению с носителями без мутации (медиана 12 кОд/мл; диапазон от 8,9 до 17,7 кОд/мл) (рисунок 1).
Рисунок 1
Различия в уровнях СА 125 (Md) между женщинами с положительным и отрицательным статусом BRCA-мутации. Легенда: Результаты U-критерия Манна-Уитни, отображенные в виде гистограмм, показывают отсутствие достоверной разницы (p = .612) в уровнях СА125 у носителей мутации BRCA1/2 (положительный, оранжевая гистограмма) и носителей без мутации (отрицательный, зеленая гистограмма). На оси абсцисс отложено абсолютное значение СА125 в кОд/мл. Сокращения: (Мд, медиана)
Взаимосвязь мутационного статуса BRCA1/2 и менопаузального статуса
Учитывая значительное влияние менопаузального статуса на уровень СА125, для анализа влияния мутационного статуса BRCA1/2 и менопаузального статуса на уровень СА125 был проведен двухфакторный дисперсионный анализ (ANOVA). Рассчитанные параметры приведены в таблице 4.
Таблица 4 Уровни СА125 в сыворотке крови в зависимости от статуса мутации BRCA и менопаузального статуса
| Пременопаузальный | Постменопаузальный | В целом | |||||||
| Статус BRCA мутации | С | ± СО | n | С | ± СО | n | С | ± СО | n |
| Отрицательнаяa | 15.38 | 8.50 | 496 | 12.76 | 7.85 | 343 | 14.31 | 8.33 | 839 |
| МД (ИКР) | 13.35 | (9.63; 18.84) | 10.80 | (8.30; 14.90) | 12.00 | (8.9; 17.7) | |||
| Положительнаяb | 16.72 | 10.34 | 357 | 10.06 | 4.42 | 109 | 15.16 | 9.71 | 466 |
| МД (ИКР) | 14.20 | (9.15; 21.75) | 9.40 | (6.80; 12.35) | 12.75 | (8.7; 18.75) | |||
| Всего | 15.94 | 9.33 | 853 | 12.11 | 7.26 | 452 | 14.61 | 8.86 | 1305 |
| МД (ИКР) | 13.90 | (9.45; 19.50) | 10.50 | (7.93; 14.00) | 12.00 | (8.8; 18.1) | |||
Сокращение: n Количество, С Среднее значение, СО Стандартное отклонение, мин. Минимум, макс. Максимум, Мд Медиана, ИКР Интерквартильный размах
a Отрицательный результат касается женщин без вредных мутаций в генах BRCA1 или 2
bПоложительные результаты касаются женщин без вредных мутаций в генах BRCA1 или 2
Выявлено статистически значимое взаимодействие между влиянием мутационного статуса BRCA1/2 и менопаузального статуса на уровень СА125 в сыворотке крови, F(1, 1301) = 12,986, p < 0,001. T-критерий Уэлча показал, что уровень СА125 у женщин, которые не являются носителями мутации, был значительно выше в пременопаузе, чем в постменопаузе, t (770,98) = 4,583, p <0,001 с небольшим эффектом, d = 0,32, 95% ДИ [0,18 – 0,46]. Для носителей мутации BRCA1/2 мы также обнаружили достоверно более высокие уровни СА125 у женщин в пременопаузе по сравнению с женщинами в постменопаузе, t(417.23) = 9,628, p < 0,001, но с большим эффектом, d = 1,05, 95% ДИ [0,83 – 1,28]. На рисунке 2 показаны средние уровни СА125 в зависимости от статуса BRCA-мутации и менопаузального статуса.
Рисунок 2
Уровни CA 125 (M ± 1 СО) с учетом мутационного статуса BRCA и менопаузального статуса. Условные обозначения: Гистограммы, показывающие результаты двустороннего ANOVA. A Показывает средние значения CA125 для женщин в пременопаузе без мутаций (n = 496). B Средние значения CA125 для носителей мутации BRCA в пременопаузе (n = 357). C Отображены средние значения CA125 для постменопаузальных носителей без мутаций (n = 343). D Отображены средние значения CA125 для носителей BRCA-мутации в постменопаузе (n = 109). Сокращения: ANOVA – дисперсионный анализ; С – среднее значение; СО – стандартное отклонение
Обсуждение
В нашем исследовании мы обнаружили значительно более высокие уровни СА125 у женщин в пременопаузе, чем у женщин в постменопаузе в целом. Мы наблюдали снижение уровня СА125 с увеличением возраста как у носителей BRCA-мутации, так и у носителей не-BRCA-мутации. Существовала небольшая, но значимая отрицательная корреляция между возрастом и уровнем СА125, независимо от мутационного статуса. Это наблюдение согласуется с данными современной литературы [21, 22, 31]. Согласно нашему уравнению регрессии, можно предположить, что уровень СА125 в сыворотке крови 50-летней женщины составляет 14,39 кОд/л, независимо от мутационного статуса. Подобные результаты были получены Pauler и др., которые обнаружили, что уровень СА125 у женщин в возрасте 50 лет обычно колеблется между 13 и 22 единицами/мл [21]. Интересно, что при учете мутационного статуса мы наблюдали очень небольшую, но значимую отрицательную корреляцию между возрастом и уровнем СА125 в случаях без мутации в BRCA1/2, по сравнению с умеренной отрицательной корреляцией в случаях с мутацией в BRCA1/2.
В недавнем исследовании Gschwantler-Kaulich и др. [39] было выявлено значительно более высокие уровни СА125 у женщин с мутацией в BRCA1 по сравнению с носителями без мутации. Мы не обнаружили достоверной разницы в уровнях СА125 у носителей мутации BRCA1/2 по сравнению с носителями без мутации в целом. Hermsen и соавт. также не обнаружили существенной разницы в уровнях СА125 у женщин с высоким наследственным риском по сравнению со здоровыми женщинами [31]. Ретроспективное исследование Chen и соавт. также сравнивало уровни СА125 у носителей мутации BRCA1/2 с носителями без мутации и не выявило достоверной разницы между этими группами. Однако менопаузальный статус не рассматривался в анализе как фактор, который потенциально может вызвать неправильную интерпретацию результатов [40]. Наши результаты также показывают статистически значимое взаимодействие между статусом мутации BRCA1/2 и менопаузальным статусом на уровень CA125 в сыворотке крови. Это означает, что влияние менопаузального статуса зависело от наличия мутации в BRCA1/2. Соответственно, мы наблюдали большее снижение уровня СА125 в сыворотке крови у носителей мутации в постменопаузе, чем у носителей без мутации.
В нескольких исследованиях сообщалось о значительно более низком возрасте наступления естественной менопаузы у носителей BRCA-мутации, чем у здоровых не-носителей [41, 42], что может объяснить большее снижение уровня СА125 в сыворотке крови у носителей BRCA-мутации, поскольку они уже находились бы в постменопаузе дольше. Исследование Tea и соавт. даже показало значительно более раннее начало менопаузы у носителей BRCA1-мутации по сравнению с носителями BRCA2-мутации [43]. Однако недавно проведенный мета-анализ, объединивший данные 1535 носителей BRCA1/2-мутаций и 3191 человек контрольной группы, не подтвердил гипотезу о связи между вредными мутациями в BRCA1/2 и более ранним наступлением менопаузы [44]. Однако для решения вопроса о том, насколько патогенные мутации зародышевой линии BRCA1/2 и ранняя менопауза действительно связаны, необходимо провести более тщательно спланированные исследования, поскольку на сравнение возраста наступления естественной менопаузы между носителями и неносителями мутаций BRCA1/2 могут влиять различные типы предвзятости отбора.
Современный подход к скринингу рака яичников базируется на предпосылке, что заболевание должно быть выявлено на I или II стадии для увеличения шансов на выживание, но все еще ограничен низкой чувствительностью и специфичностью [13, 15, 45]. Согласно нашим результатам и нескольким исследованиям, сообщающим о более раннем начале менопаузы у носителей BRCA-мутации [41,42,43], можно с уверенностью предположить, что снижение уровня СА125 у носителей BRCA-мутации в постменопаузе повысит чувствительность для выявления рака яичников на ранних стадиях. Тем не менее, важно помнить, что между чувствительностью и специфичностью существует определенная взаимосвязь. Поэтому, хотя некоторые исследования предполагают, что снижение порогового уровня СА125 до 50 кОд/л у женщин в постменопаузе может позволить выявить больше рака на ранней стадии, это также приведет к увеличению количества ложноположительных результатов и гипердиагностики [12, 46].
Персонализация скрининга рака яичников с помощью алгоритма, основанного на лонгитюдном анализе СА125 и частом тестировании, дала многообещающие результаты у женщин с высоким риском. Например, алгоритм риска рака яичников (АРРЯ) выявляет значительное повышение базового уровня СА125 у каждой пациентки и, таким образом, повышает вероятность раннего выявления заболевания, даже до достижения стандартного порогового уровня, при этом специфичность сохраняется за счет исключения пациенток с высоким стабильным уровнем [26]. Было высказано предположение, что включение статуса мутации BRCA в упомянутые алгоритмы и другие модели оценки риска, основанные на измерении СА125, может способствовать дальнейшей персонализации и улучшению скрининга [10, 28]. Однако, учитывая недостаточную эффективность измерения сывороточного СА125 в крупных скрининговых исследованиях [47, 48], мы не ожидаем, что этот опухолевый маркер станет валидированной частью скрининга рака яичников в ближайшее время.
Наше исследование имеет несколько ограничений. Определение менопаузального статуса исключительно на основе возраста и без измерения сывороточного ФСГ и эстрадиола может привести к неправильной интерпретации результатов. Это важно учитывать у пациенток с мутациями зародышевой линии BRCA и повышенным риском преждевременной овариальной недостаточности. Из-за ретроспективного характера этого исследования мы не смогли учесть использование оральных контрацептивов, курение и большинство сопутствующих заболеваний, которые могут влиять на уровень СА125 у здоровых женщин. Поэтому нам пришлось исключить из нашего анализа случаи со значениями более 70 кОд/л. Кроме того, мы оценивали каждое измеренное значение СА125 в сыворотке крови как отдельный случай, то есть мы не анализировали одинаковое количество сывороточных значений у каждой пациентки. Учитывая, что, как показывают исследования, каждая женщина имеет свой собственный базовый уровень СА125 [26], подход, который мы применили в нашем статистическом анализе, может оказаться проблематичным. Это исследование базируется на данных женщин, участвовавших в программе раннего выявления наследственного рака молочной железы и яичников с высоким риском. Сравнение носителей мутации BRCA1/2 с женщинами, которые не имеют высокого риска рака молочной железы или яичников, могло бы обеспечить большую значимость наших результатов.
Заключение
Наши результаты свидетельствуют о том, что уровень СА125 в сыворотке крови подвергается одинаковым изменениям, вызванным старением и менопаузой, но ведет себя по-разному у носителей мутации BRCA, чем у женщин без этой мутации. Менопаузальный статус остается основным клиническим фактором, влияющим на уровень СА125 в сыворотке крови. Мы не знаем ни одного биологического механизма, который мог бы объяснить более выраженное снижение уровня СА125 у носителей мутации BRCA1/2 с увеличением возраста.
В настоящее время нам не хватает исследований, которые бы оценивали скрининг СА125 у здоровых носителей мутации BRCA1/2. Доступная литература по этому вопросу ограничена небольшими популяциями. Наша когорта из 466 пациентов высокого риска включала 132 носителей мутации BRCA1/2 и 334 не-носителей, таким образом, представляя одну из самых больших на сегодняшний день одноцентровых исследовательских когорт для пациентов высокого риска. Насколько нам известно, это первое исследование, которое описывает уровни CA125 в сыворотке крови у здоровых носителей мутации BRCA1/2 по сравнению с не носителями, а также учитывает менопаузальный статус. Мы ожидаем, что это исследование вскоре вдохновит тщательно спланированные проспективные исследования, направленные на персонализацию скрининга CA125 у носителей мутации BRCA1/2. Полученные результаты могут привести к определению нового предельного уровня СА125 для женщин с высоким наследственным риском, особенно в постменопаузальном периоде, и улучшить скрининг рака яичников.
Аббревиатуры
ANOVA:
Двухфакторный дисперсионный анализ
CA125:
Онкомаркер яичников карбогидрат антиген 125
НРМЯ:
Наследственный рак молочной железы и яичников
РЯ:
Рак яичников
РУСО:
Риск уменьшающая сальпингоофорэктомия
ТВУ:
Трансвагинальное УЗИ
Ссылки на источники
- Lheureux S, Gourley C, Vergote I, Oza AM. Epithelial ovarian cancer. Lancet. 2019;393(10177):1240–53.
- Kuchenbaecker KB, Hopper JL, Barnes DR, Phillips KA, Mooij TM, Roos-Blom MJ, et al. Risks of breast, ovarian, and contralateral breast cancer for BRCA1 and BRCA2 mutation carriers. JAMA. 2017;317(23):2402–16.
- Paluch-Shimon S, Cardoso F, Sessa C, Balmana J, Cardoso MJ, Gilbert F, et al. Prevention and screening in BRCA mutation carriers and other breast/ovarian hereditary cancer syndromes: ESMO clinical practice guidelines for cancer prevention and screening. Ann Oncol. 2016;27(suppl 5):v103–10.
- Finch APM, Lubinski J, Møller P, Singer CF, Karlan B, Senter L, et al. Impact of oophorectomy on cancer incidence and mortality in women with a BRCA1 or BRCA2 mutation. J Clin Oncol. 2014;32(15):1547–53.
- Conte C, Pelligra S, Sarpietro G, Montana GD, Della Corte L, Bifulco G, et al. Hereditary women’s cancer: management and risk-reducing surgery. Medicina (Kaunas). 2023;59(2):300.
- Yoshida T, Takahashi K, Yamatani H, Takata K, Kurachi H. Impact of surgical menopause on lipid and bone metabolism. Climacteric. 2011;14(4):445–52.
- Honigberg MC, Zekavat SM, Aragam K, Finneran P, Klarin D, Bhatt DL, et al. Association of premature natural and surgical menopause with incident cardiovascular disease. JAMA. 2019Dec 24;322(24):2411.
- Rocca WA, Bower JH, Maraganore DM, Ahlskog JE, Grossardt BR, de Andrade M, et al. Increased risk of cognitive impairment or dementia in women who underwent oophorectomy before menopause. Obstet Gynecol Surv. 2008Jan;63(1):32–3.
- Mannis GN, Fehniger JE, Creasman JS, Vanessa LMAS, Beattie MS. Risk-reducing salpingo-oophorectomy and ovarian C screening in 1077 women after BRCA testing. JAMA Intern Med. 2013;173(2):96.
- Rosenthal AN, Fraser LSM, Philpott S, Manchanda R, Burnell M, Badman P, et al. Evidence of stage shift in women diagnosed with ovarian cancer during phase II of the United Kingdom familial ovarian cancer screening study. J Clin Oncol. 2017;35(13):1411–20.
- Sessa C, Balmaña J, Bober SL, Cardoso MJ, Colombo N, Curigliano G, et al. Risk reduction and screening of cancer in hereditary breast-ovarian cancer syndromes: ESMO Clinical Practice Guideline. Ann Oncol. 2023;34(1):33–47.
- Buys SS, Partridge E, Black A, Johnson CC, Lamerato L, Isaacs C, et al. Effect of screening on ovarian cancer mortality: The Prostate, Lung, Colorectal and Ovarian (PLCO) cancer screening randomized controlled trial. JAMA. 2011;305(22):2295–302.
- Jacobs IJ, Menon U, Ryan A, Gentry-Maharaj A, Burnell M, Kalsi JK, et al. Ovarian cancer screening and mortality in the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS): A randomised controlled trial. The Lancet. 2016;387(10022):945–56.
- Smith RA, Andrews KS, Brooks D, Fedewa SA, Manassaram-Baptiste D, Saslow D, et al. Cancer screening in the United States, 2017: a review of current American cancer society guidelines and current issues in cancer screening. CA Cancer J Clin. 2017;67(2):100–21.
- Stirling D, Evans DGR, Pichert G, Shenton A, Kirk EN, Rimmer S, et al. Screening for familial ovarian cancer: Failure of current protocols to detect ovarian cancer at an early stage according to the International Federation of Gynecology and Obstetrics System. J Clin Oncol. 2005;23(24):5589–96.
- Charkhchi P, Cybulski C, Gronwald J, Wong FO, Narod SA, Akbari MR. CA125 and ovarian cancer: a comprehensive review. Cancers (Basel). 2020;12(12):1–29.
- Akinwunmi BO, Babic A, Vitonis AF, Cramer DW, Titus L, Tworoger SS, et al. Chronic medical conditions and CA125 levels among women without ovarian cancer. Cancer Epidemiol Biomarkers Prev. 2018;27(12):1483.
- Sevinc A, Adli M, Kalender ME, Camci C. Benign causes of increased serum CA-125 concentration. Lancet Oncol. 2007;8(12):1054–5.
- Singhal A, Lander E, Karachristos A, Daly E, Dowling P, Patel V, et al. Elevation of CA 125 and CA 19–9 in patients with end-stage liver disease. Int J Biol Markers. 2012;27(2):147–51.
- Van CB, Valentin L, Van HC, Zhang J, Jurkovic D, Lissoni AA, et al. A novel approach to predict the likelihood of specific ovarian tumor pathology based on Serum CA-125: a multicenter observational study. Cancer Epidemiology and Prevention Biomarkers. 2011;20(11):2420–8.
- Pauler DK, Menon U, McIntosh M, Symecko HL, Skates SJ, Jacobs IJ. Factors influencing serum ca125ii levels in healthy postmenopausal women. Cancer Epidemiol Biomarkers Prev. 2001;10(5):489–93.
- Skates SJ, Mai P, Horick NK, Piedmonte M, Drescher CW, Isaacs C, et al. Large prospective study of ovarian cancer screening in high-risk women: CA125 cut-point defined by menopausal status. Cancer Prev Res (Phila). 2011;4(9):1401.
- Babic A, Cramer DW, Kelemen LE, Köbel M, Steed H, Webb PM, et al. Predictors of pretreatment CA125 at ovarian cancer diagnosis: a pooled analysis in the ovarian cancer association consortium. Cancer Causes Control. 2017;28(5):459.
- Bon GG, Kenemans P, Dekker JJ, Hompes PG, Verstraeten RA, Van Kamp GJ, et al. Fluctuations in CA 125 and CA 15–3 serum concentrations during spontaneous ovulatory cycles. Hum Reprod. 1999;14(2):566–70.
- Duffy MJ, Bonfrer JM, Kulpa J, Rustin GJS, Soletormos G, Torre GC, et al. CA125 in ovarian cancer: European Group on Tumor Markers guidelines for clinical use. Int J Gynecol Cancer. 2005;15(5):679–91.
- Skates SJ, Greene MH, Buys SS, Mai PL, Brown P, Piedmonte M, et al. Early detection of ovarian cancer using the risk of ovarian cancer algorithm with frequent CA125 testing in women at increased familial risk – Combined results from two screening trials. Clin Cancer Res. 2017;23(14):3628–37.
- Menon U, Gentry-Maharaj A, Hallett R, Ryan A, Burnell M, Sharma A, et al. Sensitivity and specificity of multimodal and ultrasound screening for ovarian cancer, and stage distribution of detected cancers: results of the prevalence screen of the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS). Lancet Oncol. 2009;10(4):327–40.
- Zhang L, Chen Y, Wang K. Comparison of CA125, HE4, and ROMA index for ovarian cancer diagnosis. Curr Probl Cancer. 2019;43(2):135–44.
- Jacobs IJ, Skates SJ, MacDonald N, Menon U, Rosenthal AN, Davies AP, et al. Screening for ovarian cancer: a pilot randomised controlled trial. The Lancet. 1999;353(9160):1207–10.
- Sasamoto N, Babic A, Rosner BA, Fortner RT, Vitonis AF, Yamamoto H, et al. Predicting circulating CA125 levels among healthy premenopausal women. Cancer Epidemiol Biomarkers Prev. 2019;28(6):1076.
- Hermsen BBJ, von Mensdorff-Pouilly S, Berkhof J, van Diest PJ, Gille JJP, Menko FH, et al. Serum CA-125 in relation to adnexal dysplasia and cancer in women at hereditary high risk of ovarian cancer. J Clin Oncol. 2007;25(11):1383–9.
- Meden H, Fattani-Meiodi A. CA 125 in benign gynecological conditions. Int J Biol Markers. 1998;13(4):231–7.
- Maiorana A, Cicerone C, Niceta M, Alio L. Evaluation of Serum CA 125 Levels in Patients with Pelvic Pain Related to Endometriosis. Biol Markers. 2007;22(3):200–2.
- Oliveira MAP, Raymundo TS, Soares LC, Pereira TRD, Demôro AVE. How to Use CA-125 More Effectively in the Diagnosis of Deep Endometriosis. Biomed Res Int. 2017;2017.
- Kauppila A, Telimaa S, Ronnberg L, Vuori J. Placebo-controlled study on serum concentrations of CA-125 before and after treatment of endometriosis with danazol or high-dose medroxyprogesterone acetate alone or after surgery. Fertil Steril. 1988;49(1):37–41.
- Santulli P, Streuli I, Melonio I, Marcellin L, M’Baye M, Bititi A, et al. Increased serum cancer antigen-125 is a marker for severity of deep endometriosis. J Minim Invasive Gynecol. 2015;22(2):275–84.
- Costanian C, McCague H, Tamim H. Age at natural menopause and its associated factors in Canada: Cross-sectional analyses from the Canadian Longitudinal Study on Aging. Menopause. 2018;25(3):265–72.
- Gold EB, Bromberger J, Crawford S, Samuels S, Greendale GA, Harlow SD, et al. Factors associated with age at natural menopause in a multiethnic sample of midlife women. Am J Epidemiol. 2001;153(9):865–74.
- Gschwantler-Kaulich D, Weingartshofer S, Rappaport-Fürhauser C, Zeilinger R, Pils D, Muhr D, et al. Diagnostic markers for the detection of ovarian cancer in BRCA1 mutation carriers. PLoS ONE. 2017;12(12):1–12.
- Chen Y, Bancroft E, Ashley S, Arden-Jones A, Thomas S, Shanley S, et al. Baseline and post prophylactic tubal-ovarian surgery CA125 levels in BRCA1 and BRCA2 mutation carriers. Fam Cancer. 2014;13(2):197–203.
- Finch A, Valentini A, Greenblatt E, Lynch HT, Ghadirian P, Armel S, et al. Frequency of premature menopause in women who carry a BRCA1 or BRCA2 mutation. Fertil Steril. 2013;99(6):1724–8.
- Lin WT, Beattie M, Chen L may, Oktay K, Crawford SL, Gold EB, et al. Comparison of Age at Natural Menopause in BRCA1/2 Mutation Carriers With a Non–Clinic-Based Sample of Women in Northern California. Cancer. 2013;119(9):1652.
- Tea MKM, Weghofer A, Wagner K, Singer CF. Association of BRCA1/2 mutations with FMR1 genotypes: Effects on menarcheal and menopausal age. Maturitas. 2013;75(2):148–51.
- Kępczyński Ł, Połatyńska K, Nykel A, Sałamunia J, Kałużewski T, Kużawczyk A, et al. Age of natural menopause onset in BRCA1/2 carriers – systematic review and meta-analysis. Prz Menopauzalny. 2020;19(4):171.
- Woodward ER, Sleightholme H V., Considine AM, Williamson S, McHugo JM, Cruger DG. Annual surveillance by CA125 and transvaginal ultrasound for ovarian cancer in both high-risk and population risk women is ineffective. BJOG. 2007;114(12):1500–9.
- Havrilesky LJ, Dinan M, Sfakianos GP, Curtis LH, Barnett JC, van Gorp T, et al. Costs, effectiveness, and workload impact of management strategies for women with an adnexal mass. J Natl Cancer Inst. 2015;107(1):322.
- Henderson JT, Webber EM, Sawaya GF. Screening for ovarian cancer updated evidence report and systematic review for the US preventive services task force. JAMA. 2018;319(6):595–606.
- Menon U, Gentry-Maharaj A, Burnell M, Singh N, Ryan A, Karpinskyj C, et al. Ovarian cancer population screening and mortality after long-term follow-up in the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS): a randomised controlled trial. Lancet. 2021;397(10290):2182.
Вопросы и Ответы
Какова цель данного ретроспективного когортного исследования?
- Целью исследования было оценить связь между уровнем CA125, статусом мутации BRCA1/2 и менопаузой у женщин с высоким риском рака яичников, чтобы предоставить больше информации о клинических состояниях, которые могут влиять на уровень CA125.
Какие методы были использованы в исследовании?
- В исследовании ретроспективно анализировались повторные измерения уровня CA125 и клинические данные 466 женщин с высоким риском развития рака яичников. Сравнивались уровни CA125 между женщинами с и без вредных мутаций в BRCA1/2. Для анализа использовались корреляция Пирсона, U-критерий Манна-Уитни и двухфакторный дисперсионный анализ (ANOVA).
Какова связь между уровнем CA125 и менопаузальным статусом?
- Уровень CA125 в сыворотке крови женщин в пременопаузе был значительно выше (медиана 13,8 кОд/мл), чем у женщин в постменопаузе (медиана 10,4 кОд/мл; p < .001).
Была ли выявлена достоверная разница в уровнях CA125 у носителей и неносителей мутации BRCA?
- Не было выявлено достоверной разницы в уровнях CA125 у носителей и неносителей мутации BRCA во всех возрастных группах (p = 0,612).
Как мутационный статус BRCA1/2 и менопаузальный статус влияют на уровень CA125?
- Двухфакторный дисперсионный анализ выявил значительное взаимодействие между статусом мутации BRCA1/2 и менопаузальным статусом на уровне CA125 (p < 0,001). Наблюдалась значительная разница между уровнями CA125 у женщин в пременопаузе и постменопаузе, с большим эффектом у носителей мутации BRCA (p < 0,001, d = 1,05), тогда как у носителей без мутации наблюдался лишь небольшой эффект (p < 0,001, d = 0,32).
Каковы выводы исследования относительно влияния мутаций BRCA1/2 на уровень CA125?
- Результаты исследования свидетельствуют о том, что наследственные мутации в BRCA1/2 влияют на снижение уровня CA125 с возрастом. Для подтверждения этого влияния и определения новых уровней отсечения CA125 у носителей мутации необходимы проспективные исследования.
Кто участвовал в исследовании и какие критерии отбора были использованы?
- В исследовании участвовали 466 женщин с высоким риском развития рака яичников, которые проходили скрининг в рамках программы раннего выявления наследственного рака молочной железы и яичников. Были исключены женщины с диагнозом рака яичников, неизвестным статусом мутаций BRCA1/2, без измерения CA125, а также с эндометриозом или воспалительными заболеваниями органов малого таза в анамнезе.