🤖 Краткий пересказ от ИИ
Ультразвуковое исследование является ключевым методом в диагностике патологий надпочечников у детей, начиная от их эмбриологии и нормального развития до широкого спектра заболеваний, включая опухоли, врожденные аномалии и сосудистые нарушения.
Статья подробно описывает ультразвуковые характеристики нормального и патологически измененного строения надпочечников у детей, уделяя особое внимание таким состояниям, как нейробластома, врожденная гиперплазия надпочечников и неонатальные кровоизлияния. Для эффективной диагностики рекомендуется использовать современное оборудование, например, УЗИ аппараты.
✅ Ключевые тезисы из статьи:
- Диагностика: Ультразвуковое исследование позволяет выявить широкий спектр патологий надпочечников у детей, от врожденных аномалий до опухолей.
- Лечение: Раннее ультразвуковое выявление критически важно для своевременного начала лечения и улучшения прогноза.
- Преимущества: УЗИ является неинвазивным, доступным и информативным методом для оценки надпочечников у детей.
- Ограничения: Не всегда удается точно дифференцировать доброкачественные и злокачественные образования только по УЗИ.
Последнее обновление: 22 июля 2025 р.
Экспертная проверка: Материал проверен и отредактирован экспертами RH.ua
Примечание об ИИ: Этот блок создан с помощью генеративного ИИ для быстрого ознакомления с основными идеями статьи. Для полного понимания темы рекомендуем прочесть полный текст.
⚠️ Не заменяет медицинскую консультацию
АВТОР: Rob Goodman
Отдел диагностической радиологии, Медицинской школы Йельского университета, (Нью-Хейвен, США)
КЛЮЧЕВЫЕ СЛОВА: ультразвук, надпочечники, дети, педиатрия
ОСНОВНЫЕ ПУНКТЫ
- Понимание эмбриологии надпочечников
- Определение нормальной картины надпочечников в зависимости от возраста
- Описание ультразвуковых особенностей наиболее часто встречающихся образований надпочечников
ЭМБРИОЛОГИЯ
Надпочечники состоят из двух отдельных тканей – мозгового вещества и коры. Кора надпочечников у плода возникает на 5 неделе беременности в результате пролиферации мезотелиальных клеток с обеих сторон задней брюшной стенки между корнем брыжейки плода и урогенитальным гребнем. Эта первая волна клеточной пролиферации приводит к появлению фетального слоя коры, после чего на 6-й неделе вторая волна клеточной пролиферации приводит к образованию внешнего зрелого кортикального слоя. На 8-й неделе эта двухслойное образование клеток отделяется от мезотелиальных клеток, из которых они образовались в пределах забрюшинного пространства, и в этот момент оно намного больше, чем почки плода.
Мозговое вещество надпочечников возникает из клеток нервного гребня симпатических ганглиев, которые лежат на уровне чревного сплетения. Эти хромафинные клетки начинают мигрировать на 7 неделе жизни плода по направлению к скоплению мезотелиальных клеток надпочечников и, достигнув его, проникают в его центр. В конце третьего триместра мозговое вещество надпочечников достигает полностью центрального положения. Хотя у мозгового вещества надпочечников в конечном счете различают 3 различных гистологических зоны (гломерулярная, пучковая и сетчатая), у мозгового вещества новорожденного всего 2 зоны, потому что сетчатая зона развивается постнатально через 3 года.
СТРУКТУРА
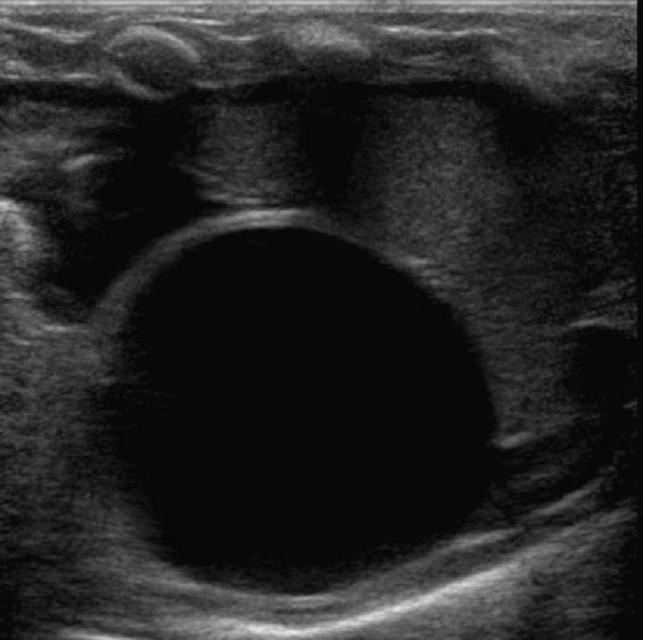
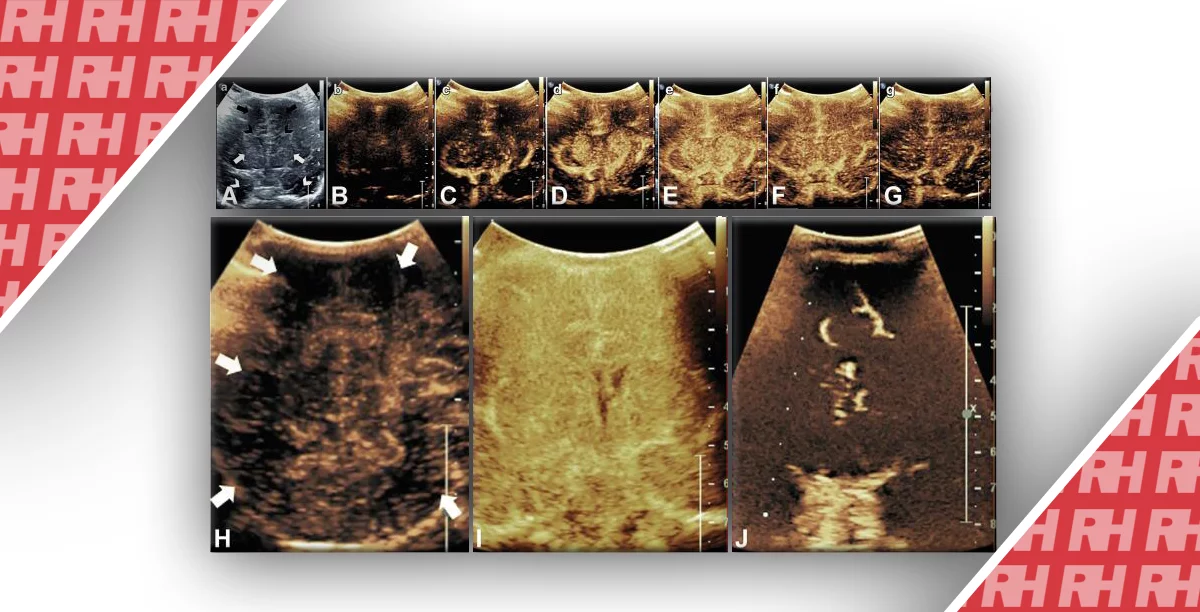
Надпочечники состоят из центрального эхогенного мозгового вещества и окружающего гипоэхогенного коркового вещества, которые легко идентифицируются в неонатальном периоде (рис.1) из-за выраженной кортикальной зоны плода, которая на этом этапе составляет 80% объема железы.
Рис. 1. Ультразвуковое изображение нормального надпочечника в неонатальном периоде. Обратите внимание на большой размер и четкую кору (короткая стрелка) и мозговое вещество (длинная стрелка).
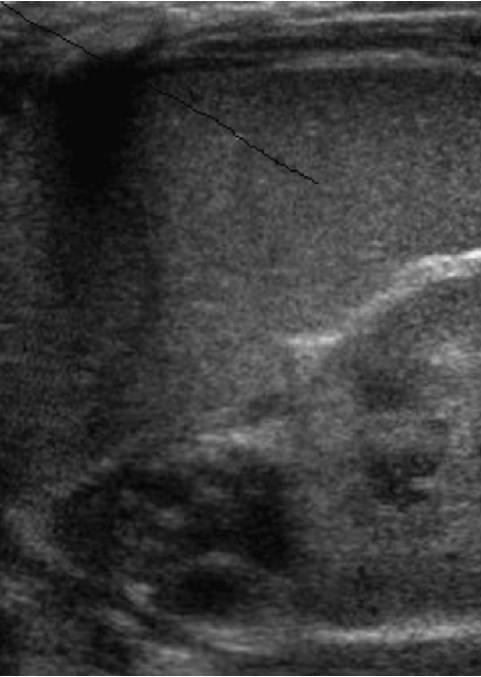
Это сонографическое различие между слоями становится менее очевидным у детей старшего возраста, когда железы принимают более равномерный гипоэхогенный вид (рис.2), из-за инволюции этой утолщенной кортикальной зоны плода в течение первых 3 недель жизни.
Рис. 2. Ультразвуковое изображение надпочечника в возрасте 5 лет. Обратите внимание на меньший размер и менее выраженную кортико-медуллярную дифференциацию (стрелка) по сравнению с рис. 1.
Постоянный зрелый кортикальный слой может идентифицироваться перед этой инволюцией в виде тонкого эхогенного периферического слоя ткани, окружающего гипоэхогенную кортикальную зону плода (рис.3).
Рис. 3. Зрелый корковый слой (стрелки) надпочечника в неонатальном периоде.
Эта физиологическая инволюция коркового слоя плода приводит к уменьшению размера железы до 50% в первые 3 недели жизни. Надпочечники лежат в забрюшинном пространстве над почками. Правый надпочечник лежит кзади и кверху верхнего полюса правой почки и ниже нижней полой вены (IVC – inferior vena cava) на уровне T11/12. Левый надпочечник обычно находится в медиальном положении на верхнем полюсе левой почки (часто доходит до почечных ворот) и, таким образом, его часто сложнее идентифицировать сонографически. Левый надпочечник также упирается в сальниковую сумку спереди, и, таким образом, это единственная область надпочечников, которая покрыта брюшиной. Надпочечники (в отличие от почек) фиксированы к периренальной фасции, так что при ультразвуковом исследовании в реальном времени, глубокое дыхание можно использовать для дифференциации этих двух органов. Почки смещаются ниже при вдохе, по сравнению с надпочечниками.
Надпочечники имеют отличительную перевернутую Y- или Т-образную форму благодаря своим 3 сегментам (рис.4).
Рис. 4. Типичная Y-образная картина нормальных надпочечников.
Эти сегменты обычно прямые у детей старшего возраста, но у новорожденных они могут быть перекрученными или выпуклыми.
Надпочечник имеет 3 основных артериальных источника: нижняя надпочечниковая артерия, возникающая из почечной артерии, средняя надпочечниковая артерия, возникающая из аорты и верхняя надпочечниковая артерия, возникающая из нижней диафрагмальной артерии. Венозный отток является важной областью для изучения и понимания, потому что он может объяснить некоторые патологические процессы, которые возникают в железе. Венозный дренаж различен для каждого надпочечника. Правая надпочечная вена впадает непосредственно в IVC, тогда как левая надпочечниковая вена входит в венозную систему через левую почечную вену.
ВРОЖДЕННЫЕ ОСОБЕННОСТИ
Из-за сложной миграции в пренатальном периоде составляющих компонентов надпочечников (описанных ранее), существует несколько врожденных особенностей надпочечников.
АГЕНЕЗИЯ НАДПОЧЕЧНИКОВ
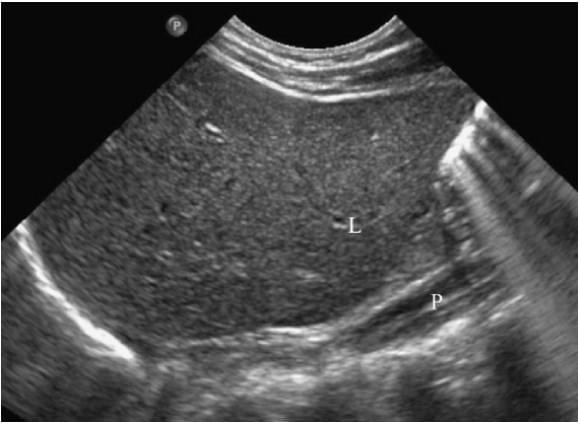
При агенезии почек, в подавляющем большинстве случаев надпочечники не затронуты. В 10% агенезии почек, однако, наблюдается сопутствующая агенезия надпочечников с отсутствием ипсилатерального надпочечника (рис.5).
Рис. 5. Отсутствие надпочечников и почек у пациента с почечной и надпочечниковой агенезией (L – печень; Р – поясничная мышца).
Хотя двустороннее агенезия надпочечников чаще всего диагностируется при аутопсии, это состояние совместимо с жизнью, если проведена соответствующая заместительная терапия. Учитывая, что если такое состояние не описано пренатально, быстрый постнатальный диагноз имеет жизненно важное значение для предотвращения неблагоприятного исхода.
ДИСКОВИДНЫЙ НАДПОЧЕЧНИК
Наиболее часто встречающаяся врожденная аномалия надпочечников – это дисковидный или блиноподобный надпочечник, который связан с ипсилатеральной почечной агенезией или почечной эктопией. Учитывая, что надпочечники и почки имеют разное происхождение (почка образуется и поднимается из таза и встречается с надпочечником во время постнатального периода), эта дисковидная форма развивается из-за отсутствия давления на надпочечник прилегающим верхним полюсом почки, что приводит к появлению дисковидного надпочечника (рис.6).
Рис.6. Дисковидный или блиноподобный надпочечник у пациента с ипсилатеральным почечным агенезом.
ПОДКОВООБРАЗНЫЙ НАДПОЧЕЧНИК
При редкой врожденной форме надпочечников, которая развивается в результате слияния обеих медиальных краев надпочечников спереди IVC, железа принимает форму подковы. Эта находка обычно связана с аспленией и правосторонним изомеризмом. аномалия также наблюдается у пациентов с дефектами нервной трубки и почечными аномалиями.
ОКОЛОПОЧЕЧНОЕ РАСПОЛОЖЕНИЕ НАДПОЧЕЧНИКОВ
Аномалии сращения надпочечников могут приводить к околопочечному расположению надпочечников, когда сегменты надпочечников образуют «лассо» вокруг верхнего полюса почки. При этом типе расположения визуальные особенности не описаны.
ЭКТОПИЧЕСКИЙ/ГЕТЕРОТОПИЧЕСКИЙ НАДПОЧЕЧНИК
Эктопический или гетеротопический надпочечник обычно обнаруживается при аутопсии у новорожденных и детей, но не описывается в литературе по визуальным методам исследования. Эти эктопические очаги обычно обнаруживаются вдоль оси слепой кишки (в связи с тем, что это эмбриональная зона происхождения надпочечников), хотя также они могут быть замечены в грудной клетке, мошонке, матке и широкой связки. Поскольку эта ткань обычно быстро поддается инволюции, она редко идентифицируется при визуализации, хотя в редких случаях эктопическая ткань надпочечников может стать гормонально активной или иметь неопластический потенциал.
ОПУХОЛИ
НЕЙРОБЛАСТОМА
Нейробластомы возникают из мозгового вещества надпочечников и являются наиболее распространенной злокачественной опухолью новорожденных и второй наиболее распространенной экстракраниальной злокачественной опухолью детского возраста. Точная идентификация этой опухоли важна, учитывая то, что нейробластомы составляют примерно 15% случаев смерти от рака у детей. Опухоли чаще всего диагностируются в возрасте 2 лет, хотя могут наблюдаться у более молодых пациентов с врожденной или перинатальной нейробластомой.
Пренатально обнаруженные супраренальные новообразования, скорее всего, представляют собой врожденную нейробластому, хотя пренатальное кровоизлияние в надпочечники и экстралобарная легочная секвестрация должны рассматриваться в плоскости дифференциального диагноза. В отличие от постнатальных проявлений нейробластомы, врожденная опухоль часто имеет кистозный компонент (рис.7), хотя твердые или частично кальцинированные поражения также описываются. Большинство врожденных нейробластом ограничены клинической картиной первой стадии и, следовательно, имеют отличный прогноз.
Рис. 7. Врожденная нейробластома в пределах меток в сагиттальной (левый) и осевой (правый) плоскостях, имеет типичные кистозные проявления.
Нейробластомы могут быть связаны с нейрофиброматозом, врожденной гиповентиляцией, болезнью Гиршпрунга и синдромом Беквит-Видеманна.
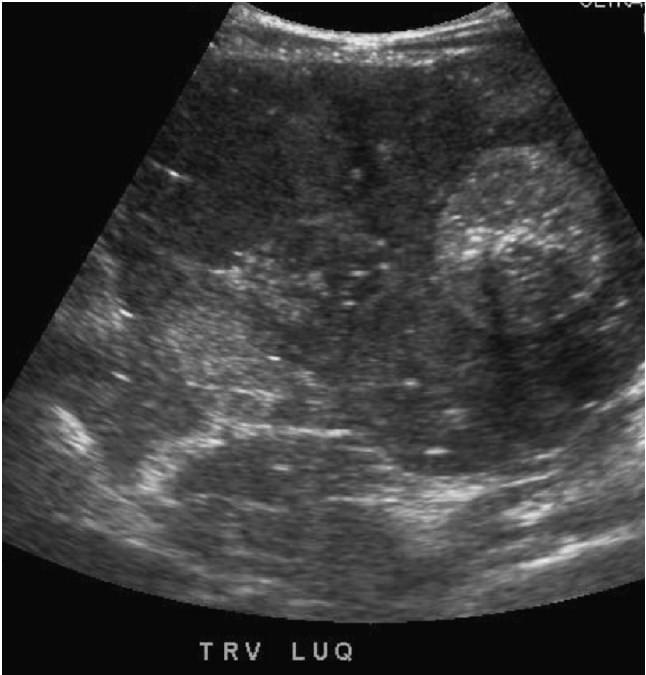
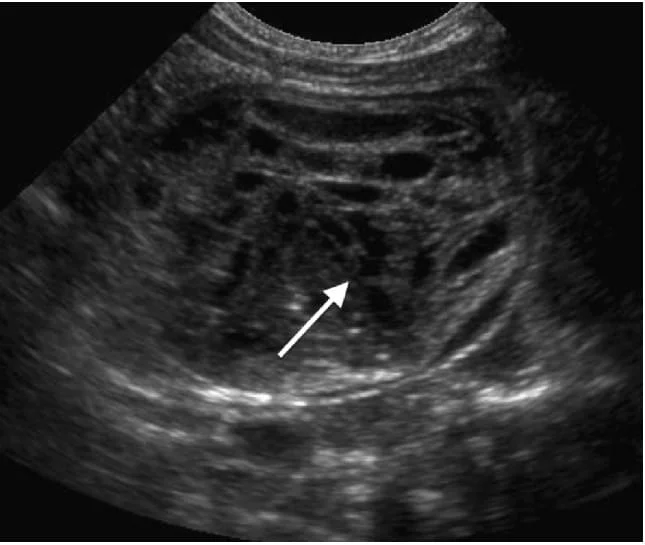
Детская нейробластома часто представлена новообразованием брюшной полости, которое определяется при пальпации, после которой ультразвуковое исследование часто выполняется в качестве первого метода визуализации. Наиболее распространенным органом происхождения нейробластомы в брюшной полости являются надпочечники, при этом по результатам ультразвукового исследования мы получаем картину гетерогенного надпочечного образования, которое часто содержит зоны кальцификации (рис.8). Области кальцификации могут быть небольшими и точечными, что, как правило, не способствует сонографическому эффекту акустического затенения (рис.9). Поражение может также содержать центральные или мультифокальные области с низким ослаблением, представляющие кистозный некроз или кровоизлияние (рис.10). Новообразование может иметь признаки инвазии в локальные структуры, такие как почка или печень, и имеет склонность к внедрению вокруг крупных сосудов (таких как чревный ствол и брыжеечная, печеночная и/или селезеночная артерии), тем самым перекрывая их (рис. 11). Из-за этого распространенного роста, как правило, определяются нейробластомы, которые приподнимают IVC и аорту от их первоначального предпозвоночного положения, в случае, когда опухоль простирается за ними (рис.12).
Рис. 8. Нейробластома надпочечников с гетерогенной эхотекстурой и зонами кальцификации.
Рис. 9. Нейробластома надпочечников с точечными, не дающими тень, эхогенными очагами, которые были областями кальцификации при гистологическом анализе.
Рис. 10. Нейробластома надпочечников с признаками центральной гипоэхогенной области (стрелка), что соответствует некрозу.
Рис. 11. Нейробластома, которая окружает прилегающие сосуды почек (стрелки).
Рис. 12. Нейробластома (крестик) приподнимает прилегающую аорту (А), в результате распространения от надпочечника в предвертебральное пространство.
Несмотря на то, что прямое кавальное распространение опухоли является опухолью Вильмса, также было описано участие этого сосуда при нейробластоме, поэтому использование цветной доплеровской визуализации необходимо для обнаружения этого редкого осложнения. Ультразвуковое сканирование в реальном времени для демонстрации движения между образованием и смежными структурами (чаще всего с печенью) также может помочь определить вероятность локальной инвазии. Если независимое движение не может быть убедительно показано между двумя структурами, вероятно, имеет место локальная инвазия.
ГАНГЛИОНЕВРОМА/ГАНГЛИОНЕЙРОБЛАСТОМА
Ганглионеврома и ганглионейробластома также являются заболеваниями нейробластической группы, возникающей из клеток нервного гребня, но, в отличие от нейробластомы, они содержат более дифференцированные маленькие круглые клетки и, следовательно, с меньшей вероятностью, будут иметь признаки злокачественности. Ганглионевромы полностью расположены в доброкачественной части нейробластического спектра, тогда как ганглионейробластомы все-таки имеют какой-то злокачественный потенциал.
Примерно одна треть ганглионейробластом возникает из надпочечников, остальные развиваются в другом месте забрюшинного пространства, заднем средостении или голове и шеи. Сонографические признаки схожи с таковыми при нейробластоме (рис.13).
Рис. 13. Ганглионейробластома надпочечника (крестик).
Ганглионевромы в надпочечниках встречаются редко, но могут трансформироваться из злокачественной нейробластомы. Учитывая доброкачественность этих поражений, они обычно идентифицируются при ультразвуковом исследовании случайно у бессимптомных пациентов-детей старшего возраста, однако распространение в забрюшинном пространстве до смежного отверстия спинномозгового нерва, может привести к неврологической симптоматике компрессии спинного мозга.
Сонографические проявления включают овоидное, твердое поражения, которое имеет повышенную эхогенность и может содержать очаги кальцификации. Локальный край или язычок ткани можно идентифицировать при ультразвуковом исследовании (рис. 14), поскольку опухоль распространяется на подлежащие отверстия спинномозговых нервов, и эта особенность, как правило, помогает в диагностике и лечении.
Рис. 14. Ретроперитонеальная ганглионеврома распространяется в соседние отверстия спинномозговых нервов (стрелки).
КОРТИКАЛЬНАЯ ОПУХОЛЬ НАДПОЧЕЧНИКОВ
Спектр первичных опухолей коры надпочечников отличается у детей и у взрослых, потому что аденомы и карциномы в педиатрической популяции трудно отличить гистологически и радиологически друг от друга. Кроме того, эти опухоли более склонны к эндокринологической активности по сравнению со взрослыми, и обычно диагностцируется во вторую очередь на фоне признаков и симптомов секреции глюкокортикоидов, минералокортикоидов, андрогенов или эстрогенов. Как таковой, термин «кортикальная опухоль надпочечников» лучше подходит к этой популяции пациентов. Эти надпочечниковые образования встречаются редко у детей, с частотой развития в год 0,3 на миллион в возрасте до 15 лет. Хотя описаны врожденные опухоли коры надпочечников, пациенты с этой патологией обычно диагностируются примерно в возрасте 5 лет, обычно это женщины, которые обычно имеют признаки или симптомы секреции гормонов, а именно признаки вирилизации/феминизации или синдрома Кушинга. Предрасполагающие факторы к развитию новообразований надпочечников включают в себя синдром Беквит-Видеманна и синдром Ли-Фраумени.
Ультразвук – идеальный инструмент, с помощью которого можно исследовать детей с соответствующими клиническими проявлениями, для исключения опухоли коры надпочечников. Эти овальные поражения надпочечников имеют обычно большие размеры (диаметром до 22 см) и дольчатую границу (рис. 15), с дольками, содержащими тонкую эхогенную капсулу. Небольшие поражения чаще являются гомогенными и имеют сходную эхогенность с почечной корой. Тогда как более крупные опухоли (> 6 см) обычно имеют центральные некротические изменения и более гетерогенную картину (рис.16).
Рис.15. Новообразование коры надпочечников (крестик) с дольчатой границей.
Рис.16. Большое новообразование коры надпочечников с центральным некрозом и гетерогенной картиной.
Кальцификация наблюдается только в одной пятой части всех опухолей. Дифференциальная диагностика доброкачественной аденомы от злокачественной карциномы достоверно может быть проведена на основе ультразвукового исследования у детей, в случае признаков сосудистой инвазии (с распространением опухоли в IVC) или метастазами (обычно в печень). Злокачественные опухоли адренокортикального типа также метастазируют в легкие и кости, хотя они не определяются с помощью ультразвука, и требуют дополнительной поперечной проекции.
ФЕОХРОМОЦИТОМА
Феохромоцитомы возникают из хромафиновых клеток мозгового вещества надпочечников и обычно выделяют катехоламины. Манифестация у детей обычно происходит в подростковом возрасте с признаками гипертонии, хотя описаны и другие типичные симптомы секреции катехоламина, такие как головные боли, сердцебиение и потоотделение. Ассоциированные с данной патологией синдромы включают в себя: нейрофиброматоз 1, туберальный склероз, синдромы Штурге-Вебера и Фон Хиппел-Линдау, а также множественные виды эндокринной неоплазии 2а и 2b, хотя большинство случаев в педиатрии являются спорадическими.
Большинство феохромоцитом (70%) у детей возникают внутри надпочечников, хотя билатеральное, множественное и вненадпочечниковое расположение встречаются чаще у детей, чем у взрослых. Например, у четверти детей (в частности, у пациентов с предрасполагающими синдромами [описанными ранее]) наблюдается двустороннее поражение железы.
При ультразвуковом исследовании феохромоцитома надпочечников определяется обычно от 2 см до 5 см в диаметре при визуализации. Обычно это гипоэхогенное, округлое образование, четко выраженное и, как правило, однородное (рис.17), хотя иногда наблюдается центральный некроз и кальцификация, особенно когда гиперваскуляризированная опухоль подвергается геморрагическому некрозу.
Рис.17. Феохромоцитома надпочечников.
МЕТАСТАЗЫ
Дискретные метастазы в надпочечники у детей чрезвычайно редки. Чаще всего происходит непосредственное прорастание смежных опухолей почек, печени и забрюшинного пространства.
КИСТЫ
Простые кисты надпочечников являются бессимптомными, редкими у детей и обнаруживаются случайно. Гистологически это обычно эндотелиальные кисты и обнаруживаются при аутопсии у 2% в педиатрической популяции. Типичные проявления при ультразвуковом исследовании включают анэхогенные, тонкостенные округлые структуры без твердых компонентов и отсутствием васкуляризации при цветной доплерографии (рис.18).
Рис.18. Киста надпочечника.
ТЕРАТОМА
Хотя зрелые тератомы являются распространенной опухолью у детей, те, которые возникают из надпочечников, встречаются редко. Эти опухоли содержат ткань, которая возникает из эктодермы, мезодермы и энтодермы и, как таковая, почти всегда содержит жир. Известны случаи развития пренатальной тератомы надпочечников.
ЗЛОКАЧЕСТВЕННАЯ РАБДОИДНАЯ ОПУХОЛЬ
Хотя злокачественная рабдоидная опухоль обычно возникает из почек, опухоли, возникающие из надпочечников, были описаны с ультразвуковыми особенностями, аналогичными тем, которые наблюдаются при нейробластоме.
СОСУДИСТАЯ ПАТОЛОГИЯ
НЕОНАТАЛЬНОЕ КРОВОИЗЛИЯНИЕ
Идиопатическое неонатальное кровоизлияние является характерным и встречается в 4 раза чаще, чем нейробластома. Его развитие связано с недоношенностью, продолжительными родами, сепсисом и аномалиями коагуляции. Источником кровоизлияния у новорожденных считается быстрая инволюция фетальной коры. Хотя неонатальное кровоизлияние часто идентифицируются случайно, такие дети могут иметь симптомы желтухи, анемию, низкое кровяное давление и/или ощутимое образование при особенно большом кровоизлиянии, хотя, даже при больших кровотечениях, недостаточность надпочечников встречается редко. Неонатальные надпочечниковые кровоизлияния чаще встречаются в правой железе из-за прямой компрессии на нее соседней большой частью печени, а также из-за склонности к любому передаточному повышенному венозному давлению, которое может быть передано непосредственно органу через правую надпочечную вену. Венозный отток из левого надпочечника обеспечивает некоторую защиту от повышенного венозного давления, поскольку он осуществляется более опосредовано через левую почечную вену.
При ультразвуковом исследовании острое кровоизлияние в надпочечники у новорожденных принимает вид неправильного эхогенного образования, которое нарушает нормальную архитектуру надпочечника (рис. 19).
Рис. 19. Неонатальное кровоизлияние в надпочечники.
Кровоток при цветной доплерографии не определяется. По мере прогрессирования заболевания и разжижения сгустка, эхогенное образование становится меньше и более гипоэхогенным, при этом могут развиваться кистозные изменения (рис.20), с возможной ревизуализацией нормальной картины надпочечников.
Рис.20. Разжижение неонатального кровоизлияния в надпочечники (крестик).
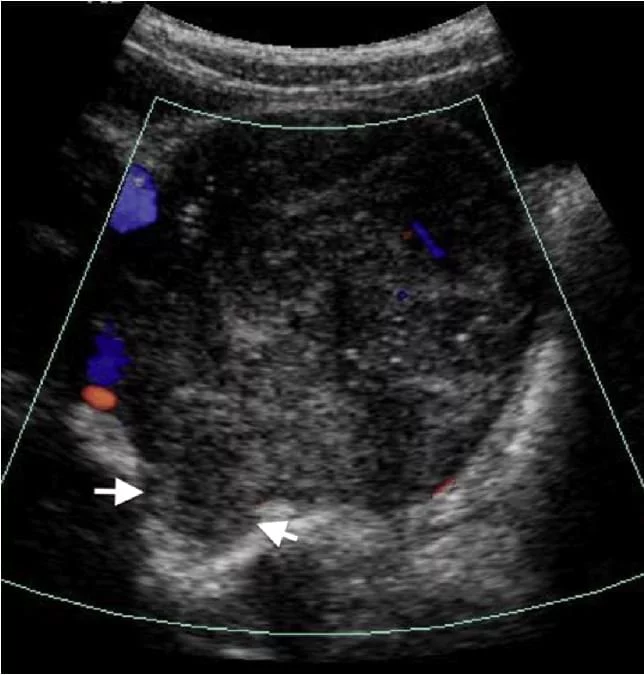
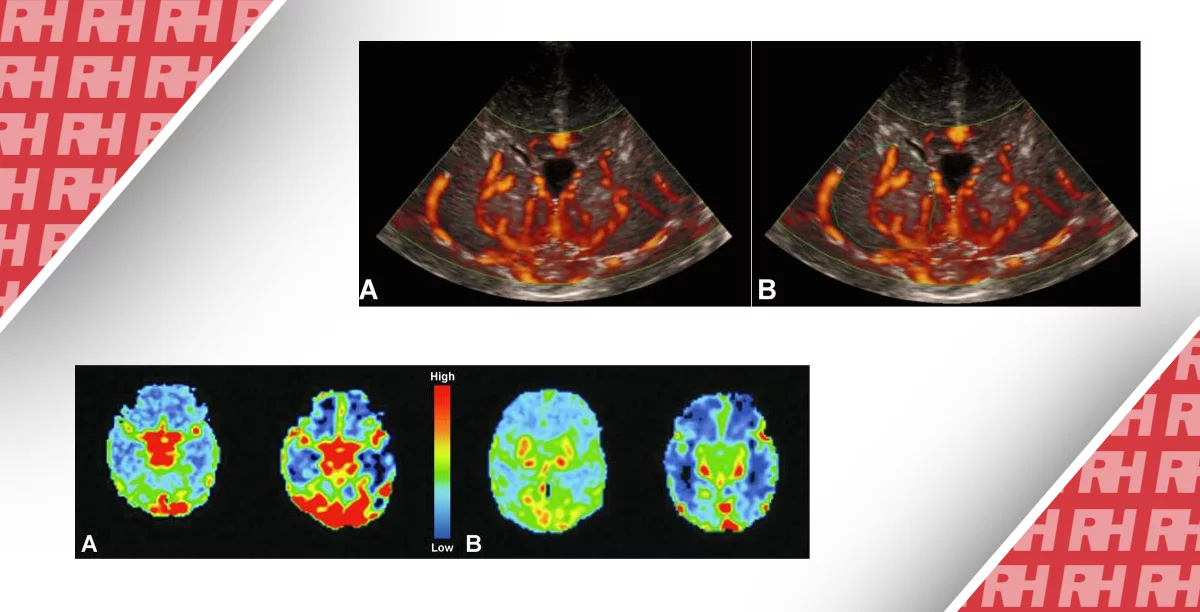
Важная роль рентгенолога заключается в том, чтобы иметь возможность представить некоторые критерии визуализации, которые помогают отличить идиопатическое неонатальное кровоизлияние от врожденной нейробластомы (которая также может кровоточить). Отсутствие потока на доплеровском изображении характеризует кровотечение над новообразованием (рис.21), также как и последовательные ультразвуковые исследования, которые демонстрируют уменьшение размера новообразования надпочечника. Это уменьшение размера обычно продолжается до полной регрессии от 20 до 165 дня жизни.
Рис. 21. Неонатальное кровоизлияние в надпочечники. Показано отсутствие цветного доплеровского потока.
ТРАВМАТИЧЕСКОЕ КРОВОТЕЧЕНИЕ
Надпочечниковое кровоизлияние может возникать как при случайной, так и при спровоцированной травме. При случайной травме это происходит примерно в 3% случаев и связано с другими ипсилатеральными торакальными и внутрибрюшными повреждениями. Картина спровоцированной тупой травмы живота может иметь признаки кровоизлияния в надпочечники. Дети, которые подвергались насилию, с подобными находками также имеют ипсилатеральные травмы ребер и внутренних органов. Сонографические особенности сходны с неонатальным идиопатическим кровоизлиянием (рис. 22).
Рис. 22. Травматическое кровоизлияние в надпочечники у 8-летнего мальчика
МЕТАБОЛИЧЕСКАЯ ПАТОЛОГИЯ
ВРОЖДЕННАЯ ГИПЕРПЛАЗИЯ НАДПОЧЕЧНИКОВ
Врожденные гиперплазии надпочечников представляют собой группу аутосомно-рецессивно наследственных дефектов ферментов надпочечников. Недостатком фермента чаще всего является 21-гидроксилаза, которая превращает 17-гидроксипрогестерон в 11-дезоксикортизол. Последствия этого дефекта фермента в биохимическом синтезе кортизола приводят к недоразвитию гениталий у девочек или сольтеряющему кризу у новорожденных любого пола. Диагноз подтверждается выявления повышенных сывороточных уровней 17-гидроксипрогестерона и исследованием кариотипа. Однако сонографический анализ надпочечников также показывает эффективность для постановки предположительносго диагноза, что может быть полезным, в то время готовятся официальные результаты.
В крупнейшем на сегодняшний день исследовании, аномальные проявления надпочечников были выявлены у 92% младенцев с нелеченой врожденной гиперплазией надпочечников. Наиболее частой сонографической находкой является дольчатый, зубчатый или мозжечковый край надпочечника. Пораженные железы также часто имеют усиленную эхогенность, с потерей непрерывной центральной эхогенной кортикальной полоски, которая заменяется пунктирной эхогенной картиной. Надпочечники при этом, как правило, увеличены (рис.23) с одним поперечным измерением более 4 мм.
Рис.23. Утолщенный надпочечниковый край (крест) в случае врожденной гиперплазии надпочечников.
ЗАБОЛЕВАНИЕ ВОЛЬМАНА
Заболевание Вольмана (первичный семейный ксантоматоз) обусловлено недостатком фермента кислой липазы, которая разрушает триглицериды и сложные эфиры холестерина. Дефект этого фермента, следовательно, приводит к увеличению уровней сложных липидов, которые осаждаются в печени, селезенке, лимфатических узлах, коре надпочечников и кишечнике. Это аутосомно-рецессивное заболевание, которое представляет собой нарушение развития организма, органомегалию и мышечную кахексию. Отложение сложных липидов в надпочечниках может образовывать скопление жирных кислот, которые в конечном счете кальцифицируются. Сетчатая зона и внутренний пучковый слои кальцифицируются с сохранением гломерулярной зоны. Причины кальцификации надпочечников показаны во вставке 1, но при болезни Вольмана кальцификация является двусторонней, железы сохраняют свою треугольную конфигурацию, что позволяет отличить этот процесс от других причин.
|
Вставка 1 Причины кальцификации надпочечников у детей |
|
ИНФЕКЦИЯ
СИНДРОМ УОТЕРХАУС-ФРИДРИХСЕНА
Синдром Уотерхаус-Фридрихена был впервые описан в 1911 году и состоит из молниеносной бактериемии (обычно менингококковой) в сочетании с пурпурной сыпью и массивными двусторонними кровоизлияниями в надпочечники. Впоследствии были выявлены другие инфекционные агенты, которые также приводят к аналогичным явлениям: пневмококк, гемолитический стрептококк и стафилококк. Сонографическая оценка надпочечников показывает изменения, аналогичные другим причинам, ранее описанного кровоизлияния в надпочечники, а именно гипоэхогенные, смешанные или преимущественно эхогенные супраренальные поражения. Кальцификация происходит через несколько недель после повреждения. Было высказано предположение, что, хотя надпочечниковая недостаточность не всегда встречается при синдроме Уотерхауса-Фридрихсена, раннее распознавание значительного повреждения надпочечников при ультразвуковом исследовании может быть полезным из-за преимуществ раннего лечения заместительной терапией кортикостероидами.
ГРАНУЛЕМАТОЗНАЯ БОЛЕЗНЬ
Гранулематозная инфекция (как правило, туберкулез) надпочечников у детей редкая находка и, как известно исторически, приводит к развитию надпочечниковой недостаточности или болезни Аддисона. Однако самый большой современный обзор надпочечниковой недостаточности на сегодняшний день у детей в Соединенных Штатах не выявил никакой инфекционной этиологии. Однако, неонатальный распространенный герпес и цитомегаловирусная инфекция описаны, как причины недостаточности надпочечников, последняя из которых может проявляться двусторонней кальцинацией надпочечников.
АБСЦЕСС НАДПОЧЕЧНИКОВ
Абсцессы надпочечников развиваются в неонатальном периоде либо de novo с бактериемическим отсевом в железе, либо как осложнение идиопатического неонатального кровоизлияния в надпочечники. Ультразвуковые описания проявлений аналогичны описанию абсцессов в другом месте, а именно: супраренальное, толстостенное кистозное поражение, которое содержит подвижные эхогенные частицы.
РЕЗЮМЕ
Точное и всестороннее знание сонографических данных при патологии надпочечников у детей жизненно необходимо для современного практикующего специалиста ультразвуковой диагностики. В этой статье описываются проявления множественных патологий надпочечников, которые могут быть использованы для оценки нарушений надпочечников у детей, которые встречаются в педиатрической радиологической практике. Для проведения исследований рекомендуем использовать аппарат от компании GE Voluson E8.
Вопросы и Ответы (FAQ)
Какова эмбриология надпочечников у детей?
- Надпочечники состоят из мозгового вещества и коры.
- Кора надпочечников формируется из мезотелиальных клеток задней брюшной стенки, начиная с 5-й недели беременности.
- Мозговое вещество происходит из клеток нервного гребня симпатических ганглиев, мигрирующих к надпочечникам с 7-й недели беременности.
- В конце третьего триместра мозговое вещество располагается центрально.
Как выглядит нормальный надпочечник у детей при ультразвуковом исследовании?
- У новорожденных надпочечники имеют центральное эхогенное мозговое вещество и окружающее гипоэхогенное корковое вещество.
- Эта дифференциация слоев становится менее выраженной у детей старшего возраста из-за инволюции корковой зоны.
- В более старшем возрасте надпочечники приобретают более однородный гипоэхогенный вид.
- Надпочечники обычно имеют перевернутую Y- или Т-образную форму.
Каковы особенности расположения надпочечников у детей?
- Правый надпочечник расположен кзади и кверху верхнего полюса правой почки, ниже нижней полой вены (на уровне T11/12).
- Левый надпочечник чаще находится медиально на верхнем полюсе левой почки, иногда достигая почечных ворот, и его сложнее идентифицировать.
- Левый надпочечник также прилежит к сальнику спереди, будучи единственной его покрытой брюшиной частью.
- Надпочечники фиксированы к периренальной фасции, что отличает их от почек при дыхательных движениях (почки смещаются больше при вдохе).
Какие врожденные аномалии надпочечников встречаются у детей и как они выглядят при УЗИ?
- Агенезия надпочечников: Отсутствие одного или обоих надпочечников, часто в сочетании с агенезией почек.
- Дисковидный надпочечник: Блиноподобная форма, связанная с агенезией или эктопией почки из-за отсутствия давления со стороны почки.
- Подковообразный надпочечник: Редкая форма, когда медиальные края надпочечников сливаются спереди от нижней полой вены, часто связана с аспленией.
- Околопочечное расположение: Сегменты надпочечника формируют “лассо” вокруг верхнего полюса почки.
- Эктопический/Гетеротопический надпочечник: Обнаруживается вдоль оси слепой кишки или в других локализациях, редко идентифицируется при визуализации.
Что такое нейробластома надпочечников и каковы ее ультразвуковые признаки у детей?
- Нейробластома — наиболее частая злокачественная опухоль новорожденных, возникающая из мозгового вещества надпочечников.
- Чаще диагностируется в возрасте до 2 лет, но может быть врожденной.
- Врожденные нейробластомы часто имеют кистозный компонент, тогда как постнатальные — гетерогенную структуру с зонами кальцификации.
- Ультразвук показывает гетерогенное образование надпочечника, часто с кальцификацией (может не давать тень), центральным некрозом или кровоизлиянием.
- Опухоль может инвазировать соседние структуры (почки, печень) и сосуды, приподнимая аорту или нижнюю полую вену.
Какие еще опухоли надпочечников могут возникать у детей и как их отличить?
- Ганглионеврома/Ганглионейробластома: Опухоли нейробластической группы, но с более дифференцированными клетками. Могут иметь повышенную эхогенность, очаги кальцификации, овоидную форму.
- Кортикальная опухоль надпочечников: Редко встречаются у детей, часто связаны с гормональной активностью. Могут быть овальными, большими, с дольчатой границей и центральным некрозом в крупных образованиях.