Резюме
Вопрос исследования
Дает ли перенос замороженных эмбрионов в цикле искусственно подготовленного эндометрия (ПЗЭ-ЗГТ) одинаковую клиническую частоту наступления беременности при 7-дневном эстрогеновом прайминге по сравнению с 14-дневным?
Дизайн (Конструкция)
Это одноцентровое, рандомизированное, контролируемое, открытое пилотное исследование. Все циклы ПЗЭ-ЗГТ были проведены в третичном центре в период с октября 2018 года по январь 2021 года. В целом 160 пациентов были рандомизированы в соотношении 1:1 на две группы по 80 пациентов в каждой: группа А (7 дней Е2 перед введением P4) и группа В (14 дней Е2 перед введением P4). Обе группы получили одиночные эмбрионы на стадии бластоцисты на 6-й день вагинального введения P4. Первичным результатом была целесообразность такой стратегии, которую оценивали по клинической частоте наступления беременности, вторичными – биохимическая частота наступления беременности, частота выкидышей, частота рождения живых детей и уровень гормонов в сыворотке крови в день проведения ПЗЭ. Химическую беременность оценивали с помощью анализа крови на ХГЧ через 12 дней после ПЗЭ, а клиническую беременность подтверждали с помощью трансвагинального УЗИ на 7 неделе.
Результаты
В анализ было включено 160 пациенток, которые были рандомизированы в группу А или группу Б на седьмой день цикла ПЗЭ-ЗГТ, если измеренная толщина эндометрия превышала 6,5 мм. После неудачного скрининга и отсева 144 пациентки были окончательно включены в группу А (75 пациенток) или группу В (69 пациенток). Демографические характеристики обеих групп были сопоставимы. Частота наступления биохимической беременности составила 42,5% и 48,8% для группы А и группы В соответственно (p 0,526). Относительно клинической частоты наступления беременности в сроке 7 недель, то статистической разницы не наблюдалось (36,3% против 46,3% для группы А и группы В соответственно, р = 0,261). Вторичные результаты исследования (биохимическая беременность, выкидыш и частота живорожденности) были сопоставимы между двумя группами для намерения лечения, так же как и значение P4 в день проведения ПЗЭ.
Заключения
В цикле переноса замороженных эмбрионов с искусственной подготовкой эндометрия 7 и 14 дней эстрогенного прайминга сопоставимы с точки зрения клинической частоты наступления беременности; преимущества семидневного протокола включают более короткое время до беременности, меньшее влияние эстрогенов, большую гибкость планирования и программирования, а также меньшую вероятность рекрутирования фолликула и спонтанного всплеска ЛГ. Важно помнить, что это исследование было разработано как пилотное с ограниченной исследуемой популяцией, поэтому оно было недостаточно мощным, чтобы определить преимущество одного вмешательства над другим; для подтверждения наших предыдущих результатов необходимы более масштабные РКИ.
Вступление
Количество циклов переноса замороженных эмбрионов (ПЗЭ) возросло с тех пор, как в 1983 году было сообщено о первой беременности в результате ЭКО с использованием криоконсервированных эмбрионов [38]. Хотя изначально перенос замороженных-размороженных эмбрионов был разработан для выполнения переноса эмбрионов в циклах донорства ооцитов [21], впоследствии оно превратилось в факультативную методику для пациенток с избыточными эмбрионами и повышенным риском развития синдрома гиперстимуляции яичников [9]. Сегодня циклы ПЗЭ также применяют в случаях позднефолликулярного повышения уровня прогестерона [4, 16, 30], асинхронии эмбриона и эндометрия [34], рецидивирующих неудач имплантации [24] и предимплантационной генетической диагностики/скрининга. Эта эволюция полезности в ландшафте ПЗЭ также отражается в имеющихся на сегодняшний день данных по использованию ПЗЭ, с 93% увеличением количества процедур между 2013 и 2018 годами [11].
Тщательный анализ современных протоколов ПЗЭ является важным для того, чтобы лучше понять оптимальную стратегию ПЗЭ. ПЗЭ может происходить как в естественном, так и в искусственном цикле[23].По данным недавнего Кокрановского метаанализа [14], нет никаких доказательств в пользу использования одной схемы вместо другой. Тем не менее, учитывая минимальный мониторинг цикла, связанный с такой практикой, то есть гормональные анализы и ультразвуковое сканирование эндометрия, а также возможность применения даже у женщин без регулярных кровотечений, протокол введения экзогенных эстрогенов и прогестерона широко используется для подготовки эндометрия [42]. Однако этот подход имеет определенные недостатки, такие как стоимость, неудобство, продолжительность лечения (особенно в случае беременности) и потенциальные побочные эффекты, связанные с приемом эстрогенов, то есть повышенный тромботический риск и преэклампсия [7, 39]. На самом деле, несколько обсервационных исследований уже намекали на повышенный риск преэклампсии при применении ЗГТ для подготовки эндометрия [17, 27, 32], а большой систематический обзор [29] подтвердил эти выводы со статистической значимостью. Связь между продолжительностью эстрогенного прайминга эндометрия и повышенной частотой гипертензивных расстройств предположили Roque и соавт. [29],тогда как Shi и соавт. [35] не обнаружили различий в возникновении гипертензивных расстройств между эПЗЭ и свежим ПЭ, когда эПЗЭ проводили в естественном цикле. С другой стороны, эстрогенная стимуляция при ПЗЭ-ЗГТ активирует маркеры тромботического риска, и ограничение в использовании ненужного гормонального воздействия является важным, как недавно описали Dalsgaard и соавт. [8]. Кроме того, отмена цикла из-за спонтанной овуляции является неконтролируемым явлением, которое может произойти всегда, особенно когда препарат эстрогена длится долго, поэтому обоснование сокращения времени воздействия эстрогена потенциально может привести к уменьшению количества спонтанных овуляций и облегчению программирования цикла ПЗЭ. Однако существуют противоположные результаты, которые еще больше подчеркивают необходимость дополнительного изучения этого вопроса [5].
Сегодня большинство протоколов ПЗЭ-ЗГТ выбирают 14-дневный период приема эстрогена для имитации естественной пролиферативной фазы менструального цикла [6]. Однако немногочисленные данные свидетельствуют о том, что для пролиферации эндометрия достаточно 5-7 дней [3, 26]. Недавно Sekhon и соавт.[33], Joly и соавт. [19] и Jiang и соавт. [18] продемонстрировали в ретроспективных когортных исследованиях, включавших более тысячи пациенток, что продолжительность приема Е2 не связана ни с частотой имплантации, ни с живорождаемостью и кумулятивной живорождаемостью, а также с уровнем эстрадиола в день начала приема прогестерона [22].
Кроме очень открытой дискуссии об идеальной продолжительности введения Е2 и недавних результатов, которые показывают, что это не влияет на результат ПЗЭ, мы должны рассмотреть еще один важный вопрос цикла ПЗЭ, а именно – задержка беременности. Недавнее исследование перспектив пациенток относительно элективного ПЗЭ (эПЗЭ) показало, что отсрочка переноса эмбрионов является важным решающим фактором в выборе эПЗЭ по сравнению с переносом свежих эмбрионов [37]. Учитывая эти важные результаты, сокращение времени до наступления беременности (ВНБ) в протоколе ПЗЭ-ЗГТ, таким образом, повысит комфорт пациенток при выборе эПЗЭ вместо свежего ПЭ. Учитывая абсолютно произвольное решение о проведении 14-дневной эстрогенной подготовки эндометрия в циклах ПЗЭ-ЗГТ, а также новые доказательства того, что продолжительность воздействия эстрогена не влияет на показатели успешности, и учитывая реальную потребность в сокращении времени до наступления беременности у пациенток, планирующих ЭКО, целью пилотного исследования было оценить целесообразность короткой подготовки эндометрия в циклах ПЗЭ-ЗГТ; Основная цель этого пилотного исследования – оценить целесообразность короткой подготовки эндометрия в циклах ПЗЭ-ЗГТ с применением 7-дневного эстрогенного прайминга перед началом P4 путем сравнения клинической частоты наступления беременности со стандартным лечением (14-дневный эстрогенный прайминг).
Материалы и методы
Исследуемая популяция и дизайн исследования
Это было одноцентровое, рандомизированное, контролируемое, открытое, пилотное исследование. Женщины, которые планировали пройти ПЗЭ-ЗГТ в нашем центре, прошли скрининг и были приглашены к участию в этом исследовании. Все циклы ПЗЭ-ЗГТ были проведены в третичном референтном центре (Брюссельский центр ЭКО, Центр репродуктивной медицины, Universitair Ziekenhuis Brussel, Бельгия) в период с октября 2018 года по январь 2021 года, а период наблюдения составлял 12 недель после ПЗЭ. Мы включили всех женщин в возрасте от 18 до 40 лет с необъяснимым бесплодием и нормальной полостью матки, которым проводили ЭКО или ИЦИС с использованием протокола агониста или антагониста ГнРГ (Табл. 1).
Таблица 1 Критерии включения/исключения
| Критерии включения | Критерии исключения |
| ▪ Женщины в возрасте ≥ 18 и < 40 лет
▪ Перенос замороженных эмбрионов с искусственной подготовкой ▪ Нормальная полость матки ▪ ЭКО/ИЦИС ▪ Цикл ЭКО с агонистом или антагонистом ГнРГ ▪ Однодневный перенос 5 бластоцист ▪ Эмбрион высокого качества (по меньшей мере Bl 3BA) на момент ПЭ ▪ Участники могут быть включены в исследование только один раз |
▪ Индекс массы тела ≤ 18 и ≥ 29
▪ Предварительный диагноз СПКЯ/ПИЯ ▪ Эндометриоз 3 и 4 стадии ▪ Предварительный диагноз гидросальпинкс ▪ Системные заболевания, такие как дисфункция щитовидной железы, если их не корректировать ▪ В анамнезе повторная неудача имплантации или повторный выкидыш ▪ Циклы ПГТ-А и ПГТ-М ▪ Циклы донорства ооцитов ▪ Известен аномальный кариотип субъекта или его партнера/донора спермы, в зависимости от источника спермы, используемой для оплодотворения в этом исследовании. В случае использования спермы партнера, у которого выработка спермы серьезно нарушена (концентрация < 1 млн/мл), должен быть задокументирован нормальный кариотип, включая отсутствие микроделеции Y-хромосомы ▪ Любое известное клинически значимое системное заболевание (например, инсулинозависимый диабет) ▪ Активная артериальная или венозная тромбоэмболия или тяжелый тромбофлебит, или эти события в анамнезе ▪ Текущая или прошлая (в течение 90 дней до скрининга) привычка курить более 10 сигарет в день |
- ЭКО экстракорпоральное оплодотворение, ИЦИС интрацитоплазменная инъекция спермы, ГнРГ гонадотропин-рилизинг-гормон, ПЭ перенос эмбриона, СПКЯ синдром поликистозных яичников, ПИЯ преждевременное истощение яичников, ПГТ-А/М предимплантационное генетическое тестирование на анеуплоидию или моногенные заболевания
Кроме того, был включен только первый однократный перенос бластоцисты на 5-й день с эмбрионом отличного качества (по меньшей мере Bl 3BA). Женщины с ИМТ ниже 18 или выше 29 кг/м2, которые имели в анамнезе повторные неудачные имплантации / повторные выкидыши или с аномальным кариотипом были исключены. Аналогично, были исключены женщины, которые имели предварительный диагноз СПКЯ/ПИЯ, эндометриоз 3 или 4 стадии, гидросальпинкс или системные заболевания, такие как дисфункция щитовидной железы (если они не были скорректированы). Кроме того, были исключены циклы ПГТ-А/М и донорство ооцитов. Письменное информированное согласие получено от всех участников исследования.
Результаты исследования
Первичным результатом была клиническая беременность через 7 недель после ПЗЭ, а вторичными – положительный уровень ХГЧ, определенный через 12 дней после ПЗЭ, биохимическая частота беременности и частота выкидышей, определенная в течение первых 12 недель беременности, согласно определениям международного глоссария по репродуктивной функции [43].
Оплодотворение, оценка качества эмбрионов и криоконсервация
Оплодотворение оценивали через 16-18 часов после ЭКО/ИЦИС по наличию двух пронуклеусов, а в дальнейшем развитие эмбрионов оценивали ежедневно до криоконсервации эмбрионов на стадии дробления (3-й день) или бластоцист (5-й и 6-й дни). Криоконсервацию проводили путем витрификации с использованием закрытого устройства для витрификации с трубками высокого уровня безопасности (CBS-ViT-HS®; Cryobiosystems) с использованием комбинации диметилсульфоксида и этиленгликоля в качестве криопротекторов (Irvine Scientific Freeze Kit®; Irvine Scientific). Эмбрионы 3-х суток оценивали по количеству и симметрии бластомеров, проценту фрагментации, вакуолизации, грануляции и многоядерности. На основе всех этих параметров всем нормально оплодотворенным эмбрионам по заранее определенному алгоритму была присвоена оценка EQ, которая делится на четыре категории: отличная, хорошая, умеренная или плохая. Эти четыре категории были использованы согласно определению Racca и соавт. [28]. Свіже перенесення ембріонів або бластоцист не було включено в це дослідження. Бластоцисти оцінювали за системою, розробленою Gardner і Schoolcraft [13] на основе стадии экспансии, количества клеток, присоединяющихся к уплотнению или бластуляции, а также появления трофэктодермы (ТЭ) и внутренней клеточной массы (ВКМ). Пригодными для криоконсервирования считались такие эмбрионы: эмбрионы 3-го дня с ≥ 6 бластомерами и ≤ 50% фрагментации; 5-го и 6-го дня, полностью развернутые или вылупленные бластоцисты с ВКМ типа А/В/С и ТЭ типа А/В. В рамках этого исследования был включен только перенос 5 однодневных эмбрионов отличного качества. Витрифицированные бластоцисты оценивали (Табл. 1) после отогрева (с помощью Irvine Scientific Thaw Kit®; Irvine Scientific). ПЗЭ витрифицированной бластоцисты (5-й и 6-й дни) проводили в день отогрева.
Подготовка эндометрия, время проведения ПЗЭ и рандомизация пациенток
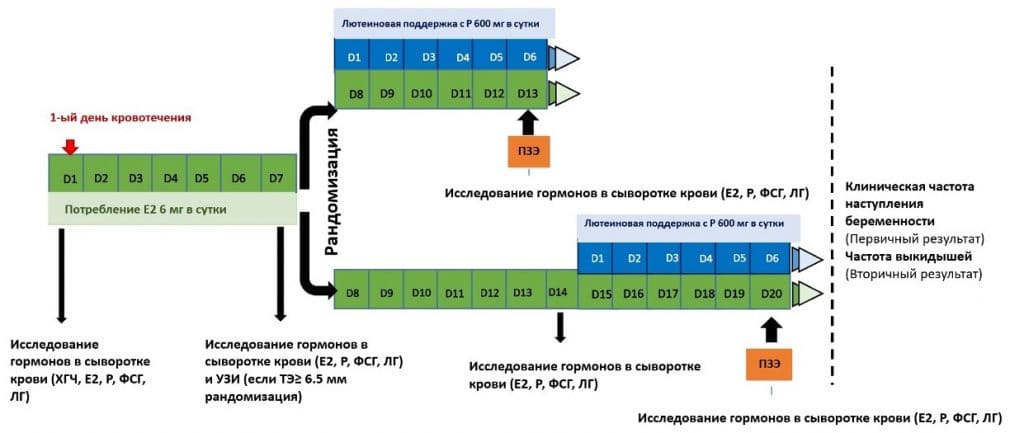
Это исследование включало только ПЗЭ в искусственно дополненном цикле (ПЗЭ-ЗГТ). Таким образом, подготовка эндометрия состояла из последовательного введения эстрадиола (Е2) валерата и микронизированного вагинального прогестерона. Пациенткам с базальными показателями гормонов, определенными как эстрадиол < 80 пг/мл и прогестерон < 1,5 нг/мл, и отсутствием кист яичников на 1-й день цикла начинали принимать 6 мг эстрадиола перорально ежедневно. На 7-й день лечения оценивали уровень гормонов в сыворотке крови и толщину эндометрия с помощью анализа крови и ультразвукового исследования соответственно. Пациенток с толщиной эндометрия ≥ 6,5 мм рандомизировали на 2 группы с распределением 1:1: группа А – 7 дней прайминга Е2, группа В – 14 дней приема Е2. Группа А начала прием 800 мг прогестерона внутривагинально в сутки (разделенных на 400 мг утром и 400 мг вечером) на 8-й день лечения и прошла ПЗЭ на 6-й день приема прогестерона. Группа Б продолжила прием эстрадиола еще 7 дней и начала принимать 800 мг интравагинального прогестерона ежедневно на 15-й день лечения Е2, а на 6-й день приема прогестерона ей провели ПЗЭ. Группа Б получала всего 20 дней приема Е2 перед ТЭ, с дополнительной оценкой показателей гормонов в сыворотке крови и толщины эндометрия на 14-й день лечения (Рис. 1).
Рис. 1 Схема дизайна исследования. Е2 (эстрадиол), Р (прогестерон), ТЭ (толщина эндометрия), ФСГ (фолликулостимулирующий гормон), ЛГ (лютеинизирующий гормон), ПЗЭ (перенос замороженных эмбрионов)
Оценка, сбор и рандомизация данных
Беременность оценивали с помощью анализа крови на уровень ХГЧ через 12 дней после ЭКО, а текущая беременность подтверждалась визуализацией сердцебиения плода во время трансвагинального УЗИ на сроке 7 недель [31]. Данные собирались в защищенной и зашифрованной eCRF, созданной специально для исследования с помощью Filemaker Pro® v13 (Filemaker Inc.) и размещенной на выделенном сервере в нашем центре (Brussels IVF). За сбор данных отвечали врачи, медицинские сестры и научные ассистенты, которые принимали участие в исследовании.
Рандомизация состоялась на 7-й день подготовки эндометрия эстрадиолом для всех пациенток с толщиной эндометрия более 6,5 мм. Рандомизацию проводили с помощью белых запечатанных непрозрачных конвертов с распределением 1:1, а случайный список генерировали с последовательными номерами с помощью программы STATA версии 15.1 (StataCorp, College Station, Техас, США). Команда медицинских сестер вместе со старшими врачами, привлеченными к исследованию, отвечала за набор, рандомизацию и распределение участников.
Размер выборки и статистический анализ
Поскольку нет доказательств в пользу применения только 7-дневного эстрадиолового прайминга при ПЗЭ-ЗГТ, формальный расчет размера выборки не проводился. Поэтому мы произвольно решили включить 160 пациенток.
Чтобы определить с 80% вероятностью преимущество одной стратегии над другой, учитывая разницу в клинической беременности в 10%, с формальным расчетом размера выборки (альфа 0,05 и бета 0,2), нам понадобилось бы 421 пациентка в каждой группе, то есть всего 842 пациентки.
Непрерывные переменные были представлены с использованием среднего значения и стандартного отклонения, тогда как категориальные характеристики, а также все первичные и вторичные результаты были представлены с использованием абсолютных и относительных значений в соответствующих группах. Непрерывные переменные анализировали с помощью U-критерия Манна-Уитни, а дихотомические переменные – с помощью точного критерия Фишера. Результаты были представлены в виде р-значений и разницы пропорций. Значение р считалось достоверным, если оно было < 0,05. Исследование проводилось в соответствии с Консорциумом пилотного исследования 2010 года [10].
Все статистические анализы были выполнены с помощью программы STATA версии 15.1 (StataCorp, Колледж Стейшн, Техас, США).
Результаты
В анализ было включено 160 пациенток, которые были рандомизированы в группу А или группу Б на 7-й день приема эстрадиола в цикле ПЗЭ-ЗГТ. После исключения отсева и неудачного скрининга 144 пациентки были включены в группу А (75 пациенток) или в группу В (69 пациенток) (Рис. 2).
Рис. 2Блок-схема рандомизации
Демографические характеристики пациенток, такие как возраст, ИМТ, АМГ, а также привычки к курению, паритет и показания к ВРТ, приведены в Табл. 2, а характеристики цикла, такие как толщина эндометрия в день начала Р4, а также Е2 и Р4 в день ПЭ, приведены в Табл. 3.
Таблица 2 Основные характеристики
| Группа А
Обработано 1 ( N = 80) |
Группа B
Контроль 0 ( N = 80) |
|
| Возраст (годы ± СО) | 33.0 ± 3.7 | 33.2 ± 3.6 |
| ИМТ(кг/м2) | 23.1 ± 2.9 | 23.9 ± 3.1 |
| АМГ (нг(мл)) | 2.8 ± 1.4 | 2.7 ± 1.9 |
| Привычка курения N (%) | ||
| - Нет | 76 (95) | 77 (96.3) |
| - Да | 4 (5) | 3 (3.8) |
| Паритет N (%) | ||
| - 0 | 28 (35) | 29 (36.2) |
| - ≥ 1 | 52 (65) | 51 (63.8) |
| Показания для проведения ВРТ | ||
| - Идиопатический (2) | 32 (40) | 40 (50) |
| - Трубный фактор (3) | 3 (3.8) | 6 (7.5) |
| - Нарушения овуляции (4) | 3 (3.8) | 2 (2.5) |
| - Мужской фактор (1) | 38 (47.5) | 26 (32.5) |
| - Эндометриоз (5) | 0 (0) | 3 (3.8) |
| - Другое (6) | 4 (5) | 3 (3.8) |
| Толщина эндометрия (мм) | 8.5 ± 1.6 | 8.5 ± 1.4 |
- Толщину эндометрия измеряли после 7 дней приема эстрогенов в группах А и Б
- ИМТ индекс массы тела, АМГ антимюллеров гормон, ВРТ вспомогательная репродуктивная технология
Таблица 3 Уровень гормонов в сыворотке крови в день ПЭ
| Группа А
( N = 80) |
Группа В
( N = 80) |
p – значение | |
| ЛГ | 5.9 ± 4.5 | 7.1 ± 6.9 | 0.259 |
| Е2 | 225.4 ± 73.8 | 228.5 ± 100.8 | 0.835 |
| Р4 | 12.8 ± 4.8 | 12.8 ± 5.2 | 0.318 |
- ЛГ лютеинизирующий гормон, Е2 эстрадиол, Р4 прогестерон
Демографические характеристики обеих групп были сопоставимы. Следует отметить, что не было существенной разницы в паритетном соотношении обеих групп. Большинство пациенток прошли один или несколько предыдущих циклов ВРТ и имели один или несколько предыдущих живых родов. Кроме того, показания к ВРТ были равномерно распределены между обеими группами. Во всей исследуемой популяции наиболее частыми показаниями к ВРТ были идиопатическая причина и мужской фактор. Не было достоверной разницы между уровнями Е2 и Р4, а также толщиной эндометрия, измеренной в день ПЭ.
Первичный результат
Результаты анализа представлены в соответствии с намерением лечения, чтобы избежать возможного смещения из-за исключенных пациентов (Табл. 4).Первичным результатом была клиническая беременность через 7 недель после ЭКО, статистической разницы между основной и контрольной группами не выявлено (36,3% против 46,3% для группы А и группы В соответственно, p = 0,261, разница пропорций 10%, 95% ДИ -0,05 – 0,25).
Таблица 4 Результаты беременности в обеих исследуемых группах (N = 160)
| Группа А
( N = 80) |
Группа В
( N = 80) |
p – значение | Разница в пропорциях | 95% ДИ | |
| Частота беременности | 34/80 (42.5) | 39/80 (48.8) | 0.526 | 0.063 | -0.09- 0.21 |
| Биохимическая беременность | 5/34 (14.7) | 2/39 (5.1) | 0.443 | -0.096 | -0.23 – 0.04 |
| Клинический показатель беременности | 29/80 (36.3) | 37/80 (46.3) | 0.261 | 0.1 | -0.05 – 0.25 |
| Частота выкидышей | 4/29 (13.8) | 3/37 (8.1) | 0.690 | -0.06 | -0.21 – 0.096 |
| Коэффициент живорожденности | 25/80 (31.3) | 34/80 (42.5) | 0.190 | 0.11 | -0.03 – 0.26 |
Вторичные результаты
Положительная частота наступления беременности составляла 42,5% и 48,8% для групп А и В соответственно (p 0,526, разница пропорций 0,6, 95% ДИ -0,09 – 0,21). Показатель биохимической беременности составлял 14,7 против 5,1 для групп А и В соответственно (р = 0,443, разница пропорций -0,096, 95% ДИ -0,23 – 0,04), а показатель выкидышей составлял 13,8 и 8,1 для групп А и В соответственно (р = 0,69, разница пропорций – 0,06, 95% ДИ -0,21 – 0-096). Коэффициент живорождаемости составил 31,3 для группы А и 42,5 для группы Б (p = 0,19, разница пропорций – 0,11, 95% ДИ -0,03 – 0,26).
Уровень гормонов в сыворотке крови в день ПЭ
Уровень эстрадиола в день ПЭ составлял 225,4 и 228,5 соответственно (р = 0,835), тогда как уровень Р4 был сопоставимым между двумя группами (12,8 нг/мл в среднем для обеих рук, р = 0,318). Уровни ЛГ также были похожими: 5,9 и 7,1 для групп А и В соответственно (р = 0,259).
Обсуждение
Насколько нам известно, это первое рандомизированное контролируемое исследование, в котором изучался более короткий период влияния эстрогенов на эндометрий (всего 7 дней) перед началом приема P4 в ВРТ с применением ЗГТ. На самом деле, существующие результаты свидетельствуют о подобной частоте клинических беременностей между 7 и 14 днями применения эстрогенов при применении ПЗЭ ЗГТ, что открывает путь к будущим более масштабным РКИ с целью подтверждения этих исследовательских результатов.
Более широкие последствия такого исследования заключаются в снижении ВНБ, что может уменьшить расходы, а также в повышении комфорта и приемлемости для пациента при выборе ПЗЭ вместо свежей ПЭ [37], а также в повышении безопасности. На самом деле, даже с точки зрения безопасности, меньшая продолжительность приема Е2 может обеспечить преимущество, связанное с возможным снижением риска тромботических и гипертензивных расстройств, связанных с протоколом ПЗЭ-ЗГТ [8].
Результаты этого исследования согласуются с ретроспективным когортным исследованием, опубликованным в 2022 году [18], в котором 4142 цикла ПЗЭ-ЗГТ были распределены в соответствии с 7 и 14 днями экспозиции эстрогена и не обнаружили разницы в кумулятивном уровне живорожденности.
Основанием для нашей гипотезы о сокращении ВНБ стала работа Navot и соавт. [25], в которой сообщается, что биологически возможно имитировать гормональную и эндометриальную среду фертильного менструального цикла и ранней гестации исключительно с помощью введения эстрогена и прогестерона. С тех пор продолжительность приема эстрогена была эмпирически выбрана на уровне 14 дней, чтобы имитировать фолликулярную фазу физиологического менструального цикла. Однако общепризнанно, что уровень Р является движущей силой, которая влияет на восприимчивость эндометрия [12, 20, 36]. Таким образом, мы не ожидали разных результатов цикла при использовании качественной бластоцисты и проведении ПЭ по протоколу, в котором менялась только продолжительность прайминга Е2.
Продолжительность введения эстрогена перед переносом замороженных эмбрионов не влияла ни на имплантацию, ни на клиническую беременность, ни на потерю беременности на ранних сроках, ни на живорожденность со статистической точки зрения, как показали Sekhon и соавт. [33] и Joly и соавт. [19]. Однако, исходя из их результатов, средняя продолжительность приема эстрогена составляла 17 и 20 дней соответственно. Результаты этого исследования совпадают с данными Sekhon и Joly и соавторов, не демонстрируя разницы в результатах между двумя группами, однако важно признать, что мы сравнивали более короткое время воздействия эстрогенов. Кроме того, мы также должны отметить, что, хотя статистически несущественная, разница в клинической беременности между двумя группами составляла около 10% в пользу 14 дней (группа B), поэтому мы рекомендуем быть осторожными в выборе такого короткого протокола, пока более масштабные исследования не подтвердят или не опровергнут наши результаты.
Наши первичные и вторичные результаты были подобными результатам популяции ПЗЭ-ЗГТ в большинстве исследований, которые сравнивали эПЗЭ со свежей ПЭ [1, 2, 40]. Показатели эстрадиола в день проведения ПЭ были сопоставимыми между двумя группами, несмотря на значительную разницу во времени экспозиции. Гормональные результаты в день ПЭ соответствовали результатам предыдущего исследования нашей группы, в котором Mackens и соавт. сообщали [22], что уровень эстрадиола не влияет на результат цикла ПЗЭ-ЗГТ.
Ограничения и преимущества
Учитывая отсутствие доказательств относительно более короткой экспозиции эстрогена во время цикла ЗГТ, мы не имели достаточно знаний и доказательств для непосредственного проведения РКИ. Поэтому основным ограничением этого исследования является то, что оно было пилотным. Из-за ограниченной численности исследуемой популяции оно не имело возможности определить преимущество одного вмешательства над другим. Вместо этого целью этого исследования было изучить тенденции по частоте наступления беременности для каждой стратегии ЗГТ и предоставить нам достаточно знаний для расчета размера выборки для дальнейших окончательных РКИ, в которых можно было бы подтвердить отсутствие преимуществ 7-дневного праймингового подхода Е2. Несмотря на то, что это пилотное исследование, эти результаты позволяют нам смело планировать большие подтверждающие РКИ, изучая безопасность и эффективность ПЗЭ-ЗГТ с целью снижения ВНБ.
Важным преимуществом этого исследования являются его строгие критерии включения, такие как выбор в пользу включения только однократного переноса бластоцист высокого качества [15, 41]. Это позволило нам достоверно сравнить влияние сокращения времени эстрогенного прайминга на результаты цикла. Кроме того, исследование было проведено в строгом соответствии с консорциумом пилотного исследования 2010 года [10].
Наконец, мы провели гормональную оценку в день ПЭ, чтобы понять возможное влияние различных протоколов на гормональные тенденции и результаты цикла, чтобы иметь полное представление о протоколе ЗГТ.
Заключения
В цикле переноса замороженных эмбрионов с искусственной подготовкой эндометрия 7 и 14 дней эстрогенного прайминга сопоставимы с точки зрения клинической частоты наступления беременности; преимущества семидневного протокола включают более короткое время до беременности, меньшее влияние эстрогенов и большую гибкость планирования и программирования, поскольку мы можем программировать с 7-8-9 днями приема эстрогенов и получить подобные результаты, даже с меньшей вероятностью рекрутирования фолликулов и спонтанного всплеска ЛГ. Таковы основные результаты этого пилотного контролируемого исследования, которые необходимо подтвердить, во-первых, с помощью показателей эндометриальных последствий, таких как молекулярная экспрессия, и, во-вторых, с помощью будущих более масштабных РКИ.
Ссылки на источники
- Aflatoonian A, Mansoori-Torshizi M, Farid Mojtahedi M, Aflatoonian B, Khalili MA, Amir-Arjmand MH, Soleimani M, Aflatoonian N, Oskouian H, Tabibnejad N, et al. Fresh versus frozen embryo transfer after gonadotropin-releasing hormone agonist trigger in gonadotropin-releasing hormone antagonist cycles among high responder women: A randomized, multi-center study. Int J Reprod Biomed. 2018;16:9–18.
- Aflatoonian A, Oskouian H, Ahmadi S, Oskouian L. Can fresh embryo transfers be replaced by cryopreserved-thawed embryo transfers in assisted reproductive cycles? A randomized controlled trial. J Assist Reprod Genet. 2010;27:357–63.
- Borini A, Dal Prato L, Bianchi L, Violini F, Cattoli M, Flamigni C. Effect of duration of estradiol replacement on the outcome of oocyte donation. J Assist Reprod Genet. 2001;18:185–90.
- Bosch E, Labarta E, Crespo J, Simón C, Remohí J, Jenkins J, Pellicer A. Circulating progesterone levels and ongoing pregnancy rates in controlled ovarian stimulation cycles for in vitro fertilization: analysis of over 4000 cycles. Hum Reprod. 2010;25:2092–100.
- Chen Z-J, Shi Y, Sun Y, Zhang B, Liang X, Cao Y, Yang J, Liu J, Wei D, Weng N, et al. Fresh versus frozen embryos for infertility in the Polycystic Ovary Syndrome. N Engl J Med. 2016;375:523–33.
- Conrad KP, Rabaglino MB, Post Uiterweer ED. Emerging role for dysregulated decidualization in the genesis of preeclampsia. Placenta. 2017;60:119–29.
- Conrad KP, von Versen-Höynck F, Baker VL. Potential role of the corpus luteum in maternal cardiovascular adaptation to pregnancy and preeclampsia risk. Am J Obstet Gynecol. 2022;226:683–99.
- Dalsgaard TH, Hvas AM, Kirkegaard KS, Jensen MV, Knudsen UB. Impact of frozen thawed embryo transfer in hormone substituted cycles on thrombotic risk markers. Thromb Res. 2022;209:23–32. https://doi.org/10.1016/j.thromres.2021.11.016. (Epub 2021 Nov 22 PMID: 34847404).
- Devroey P, Polyzos NP, Blockeel C. An OHSS-Free Clinic by segmentation of IVF treatment. Hum Reprod. 2011;26:2593–7.
- Eldridge SM, Chan CL, Campbell MJ, Bond CM, Hopewell S, Thabane L, Lancaster GA, PAFS consensus group. CONSORT 2010 statement: extension to randomised pilot and feasibility trials. BMJ. 2016;355:i5239.
- Fertility treatment 2018: trends and figures | HFEAAvailable from: https://www.hfea.gov.uk/about-us/publications/research-and-data/fertility-treatment-2018-trends-and-figures/.
- Franasiak JM, Ruiz-Alonso M, Scott RT, Simón C. Both slowly developing embryos and a variable pace of luteal endometrial progression may conspire to prevent normal birth in spite of a capable embryo. Fertil Steril. 2016;105:861–6.
- Gardner DK, Schoolcraft WB. Culture and transfer of human blastocysts. Curr Opin Obstet Gynecol. 1999;11:307–11.
- Ghobara T, Gelbaya TA, Ayeleke RO. Cycle regimens for frozen-thawed embryo transfer. Cochrane Database Syst Rev. 2017;7:CD003414.
- Glujovsky D, Farquhar C, Quinteiro Retamar AM, Alvarez Sedo CR, Blake D. Cleavage stage versus blastocyst stage embryo transfer in assisted reproductive technology. Cochrane Database Syst Rev. 2016;CD002118.
- Healy MW, Patounakis G, Connell MT, Devine K, DeCherney AH, Levy MJ, Hill MJ. Does a frozen embryo transfer ameliorate the effect of elevated progesterone seen in fresh transfer cycles? Fertil Steril. 2016;105:93-99.e1.
- Ishihara O, Araki R, Kuwahara A, Itakura A, Saito H, Adamson GD. Impact of frozen-thawed single-blastocyst transfer on maternal and neonatal outcome: an analysis of 277,042 single-embryo transfer cycles from 2008 to 2010 in Japan. Fertil Steril. 2014;101:128–33.
- Jiang WJ, Song JY, Sun ZG. Short (seven days) versus standard (fourteen days) oestrogen administration in a programmed frozen embryo transfer cycle: a retrospective cohort study. J Ovarian Res. 2022;15(1):36. https://doi.org/10.1186/s13048-022-00967-5. (PMID:35313944;PMCID:PMC8939227).
- Joly J, Goronflot T, Reignier A, Rosselot M, Leperlier F, Barrière P, et al. Impact of the duration of oestradiol treatment on live birth rate in Hormonal Replacement Therapy cycle before frozen blastocyst transfer. Hum Fertil (Camb). 2023:1–8. https://doi.org/10.1080/14647273.2022.2163467.
- Lawrenz B, Fatemi HM. Effect of progesterone elevation in follicular phase of IVF-cycles on the endometrial receptivity. Reprod Biomed Online. 2017;34:422–8.
- Legro RS, Ary BA, Paulson RJ, Stanczyk FZ, Sauer MV. Premature luteinization as detected by elevated serum progesterone is associated with a higher pregnancy rate in donor oocyte in-vitro fertilization. Hum Reprod. 1993;8:1506–11.
- Mackens S, Santos-Ribeiro S, Orinx E, De Munck N, Racca A, Roelens C, Popovic-Todorovic B, De Vos M, Tournaye H, Blockeel C. Impact of serum oestradiol levels prior to progesterone administration in artificially prepared frozen embryo transfer cycles. Front Endocrinol (Lausanne). 2020;11:255.
- Mackens S, Santos-Ribeiro S, van de Vijver A, Racca A, Van Landuyt L, Tournaye H, Blockeel C. Frozen embryo transfer: a review on the optimal endometrial preparation and timing. Hum Reprod. 2017;32:2234–42.
- Magdi Y, El-Damen A, Fathi AM, Abdelaziz AM, Abd-Elfatah Youssef M, Abd-Allah AA-E, Ahmed Elawady M, Ahmed Ibrahim M, Edris Y. Revisiting the management of recurrent implantation failure through freeze-all policy. Fertil Steril. 2017;108:72–77.
- Navot D, Laufer N, Kopolovic J, Rabinowitz R, Birkenfeld A, Lewin A, Granat M, Margalioth EJ, Schenker JG. Artificially induced endometrial cycles and establishment of pregnancies in the absence of ovaries. N Engl J Med. 1986;314:806–11.
- Navot D, Anderson TL, Droesch K, Scott RT, Kreiner D, Rosenwaks Z. Hormonal manipulation of endometrial maturation. J Clin Endocrinol Metab. 1989;68:801–7.
- Opdahl S, Henningsen AA, Tiitinen A, Bergh C, Pinborg A, Romundstad PR, Wennerholm UB, Gissler M, Skjærven R, Romundstad LB. Risk of hypertensive disorders in pregnancies following assisted reproductive technology: a cohort study from the CoNARTaS group. Hum Reprod. 2015;30:1724–31.
- Racca A, De Munck N, Santos-Ribeiro S, Drakopoulos P, Errazuriz J, Galvao A, Popovic-Todorovic B, Mackens S, De Vos M, Verheyen G, et al. Do we need to measure progesterone in oocyte donation cycles? A retrospective analysis evaluating cumulative live birth rates and embryo quality. Hum Reprod. 2020;35:167–74.
- Roque M, Haahr T, Geber S, Esteves SC, Humaidan P. Fresh versus elective frozen embryo transfer in IVF/ICSI cycles: a systematic review and meta-analysis of reproductive outcomes. Hum Reprod Update. 2019;25:2–14.
- Roque M, Valle M, Guimarães F, Sampaio M, Geber S. Freeze-all policy: fresh vs. frozen-thawed embryo transfer. Fertil Steril. 2015;103:1190–3.
- Santos-Ribeiro S, Polyzos NP, Haentjens P, Smitz J, Camus M, Tournaye H, Blockeel C. Live birth rates after IVF are reduced by both low and high progesterone levels on the day of human chorionic gonadotrophin administration. Hum Reprod. 2014;29:1698–705.
- Sazonova A, Källen K, Thurin-Kjellberg A, Wennerholm U-B, Bergh C. Obstetric outcome in singletons after in vitro fertilization with cryopreserved/thawed embryos. Hum Reprod. 2012;27:1343–50.
- Sekhon L, Feuerstein J, Pan S, Overbey J, Lee JA, Briton-Jones C, Flisser E, Stein DE, Mukherjee T, Grunfeld L, et al. Endometrial preparation before the transfer of single, vitrified-warmed, euploid blastocysts: does the duration of oestradiol treatment influence clinical outcome? Fertil Steril. 2019;111:1177-1185.e3.
- Shapiro BS, Daneshmand ST, Garner FC, Aguirre M, Ross R. Contrasting patterns in in vitro fertilization pregnancy rates among fresh autologous, fresh oocyte donor, and cryopreserved cycles with the use of day 5 or day 6 blastocysts may reflect differences in embryo-endometrium synchrony. Fertil Steril. 2008;89:20–6.
- Shi Y, Sun Y, Hao C, Zhang H, Wei D, Zhang Y, Zhu Y, Deng X, Qi X, Li H, et al. Transfer of fresh versus frozen embryos in ovulatory women. N Engl J Med. 2018;378:126–36.
- Simón C, Martín JC, Pellicer A. Paracrine regulators of implantation. Baillieres Best Pract Res Clin Obstet Gynaecol. 2000;14:815–26.
- Stormlund S, Schmidt L, Bogstad J, Løssl K, Prætorius L, Zedeler A, Pinborg A. Patients’ attitudes and preferences towards a freeze-all strategy in ART treatment. Hum Reprod. 2019;34:679–88.
- Trounson A, Mohr L. Human pregnancy following cryopreservation, thawing and transfer of an eight-cell embryo. Nature. 1983;305:707–9.
- von Versen-Höynck F, Narasimhan P, Selamet Tierney ES, Martinez N, Conrad KP, Baker VL, Winn VD. Absent or excessive corpus luteum number is associated with altered maternal vascular health in early pregnancy. Hypertension. 2019;73:680–90.
- Vuong LN, Dang VQ, Ho TM, Huynh BG, Ha DT, Pham TD, Nguyen LK, Norman RJ, Mol BW. IVF Transfer of fresh or frozen embryos in women without polycystic ovaries. N Engl J Med. 2018;378:137–47.
- Yang L, Cai S, Zhang S, Kong X, Gu Y, Lu C, Dai J, Gong F, Lu G, Lin G. Single embryo transfer by Day 3 time-lapse selection versus Day 5 conventional morphological selection: a randomized, open-label, non-inferiority trial. Hum Reprod. 2018;33:869–76.
- Younis JS, Simon A, Laufer N. Endometrial preparation: lessons from oocyte donation. Fertil Steril. 1996;66:873–84.
- Zegers-Hochschild F, Adamson GD, Dyer S, Racowsky C, de Mouzon J, Sokol R, Rienzi L, Sunde A, Schmidt L, Cooke ID, et al. The International Glossary on Infertility and Fertility Care, 2017{\dag}{\ddag}{\textsection}. Fertil Steril. 2017;32:1786–801.