Marcia M. Aracava, Rubens Chojniak, Juliana A. Souza, Almir G.V. Bitencourt., Elvira F. Marques
Department of Diagnostic Imaging, Hospital A.C. Camargo, Fundac. ao Antonio Prudente, R. Professor Antonio Prudente, 211, CEP: 01509-010 Sao Paulo, Brazil
РЕЗЮМЕ
Цель: Подтвердить перспективность прицельного ультразвукового исследования для обнаружения выявленных при МРТ патологических очагов молочной железы, которые ранее не были визуализованы при помощи маммографии, УЗИ и клинических исследований.
Методы: Это перспективное исследование включает 68 ранее не обнаруженных патологических очагов молочной железы, найдены на МРТ 49 пациентов. Критерием включения было проведение УЗИ молочной железы и маммографии ≤ 6 месяцев до МРТ. Эти патологические очаги потом прицельно осматривались повторно с помощью ультразвука до 2 недель после МРТ. МРТ исследования проводили одним или двумя радиологами (специалисты по томографии молочной железы). Патологические очаги оценивались по терминологии, описанной в шкалах BI-RADS.
Результаты: Прицельное (повторное)УЗИ определило 46/68 (67,6%) патологических очагов, найденых при МРТ исследовании. Четкой связи между данными УЗИ, типом патологического очага, размерами, морфологическими характеристиками, характеристикой контрастного усиления и данными МРТ не было. Прицельное (повторное) УЗИ определяет 100% очагов категории 5 по BI-RADS классификации, 90% очагов категории 4, и примерно 50% очагов категории 3 (p<0.05). Наблюдалась значительное совпадение (p<0.001) между данными МРТ и УЗ классификаций по шкале BI-RADS для категорий 3-5.
Выводы: Сфокусированное УЗИ может определить большую часть патологических очагов найденных при МРТ молочной железы, особенно очаги высокого риска малигнизации, в случаи его проведения профессионалом с опытом в УЗИ и МРТ молочной железы.
ВВЕДЕНИЕ
Магнитно-резонансная томография (МРТ) молочной железы за последние годы набирает значимости в связи с ее высокой чувствительностью к выявлению рака молочной железы. Частота злокачественных очагов, найденных при МРТ, но ранее не обнаруженных при физикальном осмотре и маммографии, колеблется от 6% до 34%. Не смотря на высокую чувствительность МРТ к обнаружению карцином (94-100%), наблюдается большое разногласие в литературных данных.
Как последствие низкой специфичности (37-97%), МРТ дает большое количество ложноположительных результатов. В случае обнаружения подозрительного патологического очага при МРТ, для постановки окончательного диагноза необходимо сделать перкутанную или хирургическую биопсию. Однако, вмешательства под МРТ контролем не широко доступные, дорогостоящие, и требуют затраты большого количества времени на процедуру. С другой стороны, ультразвук (УЗ) имеет несколько преимуществ над МРТ: возможность делать перкутанные биопсии под УЗ контролем, лучший доступ к определенным областям молочной железы, процедура комфортная для пациентов. Для этого вида исследований лучше купить портативный УЗИ сканер, так как его легко можно транспортировать в кабинет МРТ.
Прицельное (повторное, сфокусированное) УЗИ может определить новообразования небольших размеров, у которых отсутствуют типические ультрасонографические характеристики малигнизации. В некоторых работах исследователи оценивали способность прицельного УЗ к идентификации ранее не обнаруженных патологических очагов найденных при МРТ. Однако, все опубликованные работы были ретроспективными, а предыдущие УЗИ были сделаны не всем пациентам, что не позволяло исследователям узнать могли ли патологические очаги найдены при МРТ быть обнаружены на первоначальном УЗИ.
Целью этого перспективного исследования было подтвердить способность прицельного УЗИ к определению обнаруженных при МРТ патологических очагов молочной железы, которые были не распознаны при первой маммографии, УЗ и клиническом исследовании.
ПАЦИЕНТЫ И МЕТОДЫ
2.1. Пациенты и патологические очаги
После соглашения Совета по вопросам этики нашего учреждения, в исследование включили пациентов, которым делали МРТ молочной железы в онкологическом центре с апреля 2008 г. по ноябрь 2009г. За указанный период было сделано 640 МРТ исследований молочной железы.
Найденные 68 ранее не обнаруженные патологические очаги у 49 пациентов подлежали прицельному (повторному) УЗИ. Чтоб создать условия для истинной второй УЗ оценки, мы определили критерий включения: УЗИ молочной железы и маммография до 6 месяцев перед проведением МРТ. Возрастной диапазон пациентов был от 26 до 77 лет (медиана – 49 лет; среднее – 50,57 лет). Самыми распространёнными показания к МРТ молочной железы у этих пациентов были неубедительные маммографические/УЗИ данные (39,7%), скрининг (33,8%), и определение степени заболевания/хирургическое планирование (13,2%). Патологические очаги, найденные при МРТ, оценивали по шкале BI–RADS, разработанной Американским обществом радиологии (American College of Radiology (ACR)).
Прицельное УЗИ проводили до 2 недель после МРТ, одним или двумя радиологами с опытом в области исследованиях молочной железы. Когда обследование делали два радиолога, их мнения согласовывались. Считалось, что заключения на МРТ и УЗИ совпадали, если была корреляция строгих критериев: приблизительного размера, сходство в форме и локализации. Патологические очаги на МРТ описывали в трех плоскостях (аксиальной, сагиттальной и коронарной), чтобы способствовать определению их местонахождения при прицельном УЗИ. Другие ориентиры такие, как расстояние до соска или кожи, близкое расположение к кистам, сосудам, или к имплантатам молочной железы, также использовались для поиска местонахождения патологических очагов. Данные УЗИ анализировали по критериям предложенным Stavrosetal., окончательно классифицировали патологические очаги по ACRBI–RADS– УЗ терминологии.
МРТ проводили системой 1,5-Т (SiemensMagnetomSymphony; SiemensHealthcare, Malvern, PA), с помощью катушки,специально предназначенной для исследования молочной железы. Процедура состояла с: (1) сагиттальный Т2-взвешенный режим; (2) аксиальное Т1-взвешенное 3D градиентное эхо; (3) аксиальное пост-контраст, Т1-взвешенное 3D, жиронасыщенное градиентное эхо, динамический режим, до, и четыре раза после быстрой болюсной инъекции 0,1 ммоль/Л гадопентата димеглюмина (Magnevist; Schering, Berlin, Germany) на килограмм массы тела, с 60 секундным темпоральным разрешением; и (4) сагиттальный 3D режим высокого разрешения. После обследования, безконтрастные изображения вычитали с пост-контрастных изображений.
УЗИ проводили с помощью линейного датчика (10-12 МГц; HDI 5000, или Logiq 700; GeneralElectric; Milwaukee, WI). Целенаправленно исследовали обнаруженный при МРТ патологический очаг и оценивали его по продольной, поперечной, радиальной и противорадиальной осям.
Патологические очаги классифицировали как доброкачественные или злокачественные за гистопатологическими данными (когда они были доступны), или при повторном осмотре. Все очаги, оцененные как BI‑RADS 4 или 5 на МРТ, подлежали перкутанной или хирургической биопсии. Очаги BI–RADS 3, биопсию которых не проводили, подлежали клиническому осмотру, маммографии, УЗИ или МРТ (УЗИ для очагов обнаруженных при прицельном УЗИ; МРТ для очагов не обнаруженных при прицельном УЗИ) на протяжении одного года.
2.2. Статистический анализ
Полученные данные представлены средними величинами, стандартными отклонениями, медианами, и межквартальными интервалами. Абсолютные (n) и относительные (%) частоты, были вычислены для количественных переменных величин. Коэффициент kappa Коэна использовали для оценки совпадения заключений исследователей, которые проводили прицельное УЗИ. U-критерий Манна-Уитни (Mann–WhitneyUtest) использовали для сравнения двух групп, а односторонний дисперсионный анализ Краскела-Уоллиса (Kruskal–Wallisone–wayanalysisofvariance) – при сравнении более двух групп. Для того, чтобы подтвердить связь между качественными переменными величинами, использовали критерий согласия Пирсона (Хи-квадрат) или точный тест Фишера (chi–squaretestorFisher’sexacttest). При заключительном анализе, уровень 5% (α = 0,05) считался существенным, и все тесты были завершены, используя двусторонний критерий.
Таблица 1
Морфологические характеристики и модель контрастного усиления объёмных и необъемных образований найденных при магнитно-резонансной томографии – МРТ (n=68).
|
Параметры |
Описание |
N |
% |
| Объемное образование | |||
|
Форма
|
Округлая |
17 |
32,1 |
| Овальная |
25 |
47,2 |
|
| Лобулярная |
5 |
9,4 |
|
|
Края |
Гладкие |
43 |
81,1 |
| Неправильные |
10 |
18,9 |
|
|
Контрастное усиление |
Гомогенное |
41 |
77,4 |
| Гетерогенное |
11 |
20,8 |
|
| Периферийное |
1 |
1,9 |
|
|
Кинетика контрастного усиления |
Нарастающий |
43 |
86,0 |
| Плато |
3 |
6,0 |
|
| Вымывание |
4 |
8,0 |
|
| Необъемное образование | |||
| Распределение | Участок |
5 |
33,3 |
| Линейное |
4 |
26,7 |
|
| Протоковое |
1 |
6,7 |
|
| Сегментарное |
3 |
20,0 |
|
| Регионарное |
2 |
13,3 |
|
| Контрастное усиление | Гомогенное |
5 |
33,3 |
| Гетерогенное |
7 |
46,7 |
|
| Сгруппированное |
3 |
20,0 |
|
РЕЗУЛЬТАТИ
Со всех 68 патологических очагов найденных при МРТ, 53 (77,9%) классифицировали как объемные образования и 15 (22,1%) как необъемные образования. Их размеры были от 0,3 до 9,2 см (медиана 0,9 см; среднее 1,4 см). Частота встречаемости патологических очагов зависимо от типа, морфологических характеристик, модели контрастного усиления и BI–RADS классификация представлены в Таблице 1 и 2.
Сфокусированное УЗИ проводили два независимых радиолога, они обнаружили 63 очага (93%), что при оценке совпадения заключений показывает хорошую степень согласованности (kappa=0,617; p<0,001). 46 из 68 найденных на МРТ патологических очагов (67,6%) представлены соответствующими данными на прицельном УЗИ. По терминологии описания BI–RADS-УЗИ, 27 (58,7%) очагов классифицировали как категория 3, 16 (34,8%) – категория 4, и 3 (6,5%) – категория 5. Никаких существенных связей не наблюдалось между УЗИ-идентификацией, типом очага, размерами, морфологическими характеристиками, моделью контрастного усиления и данными МРТ.
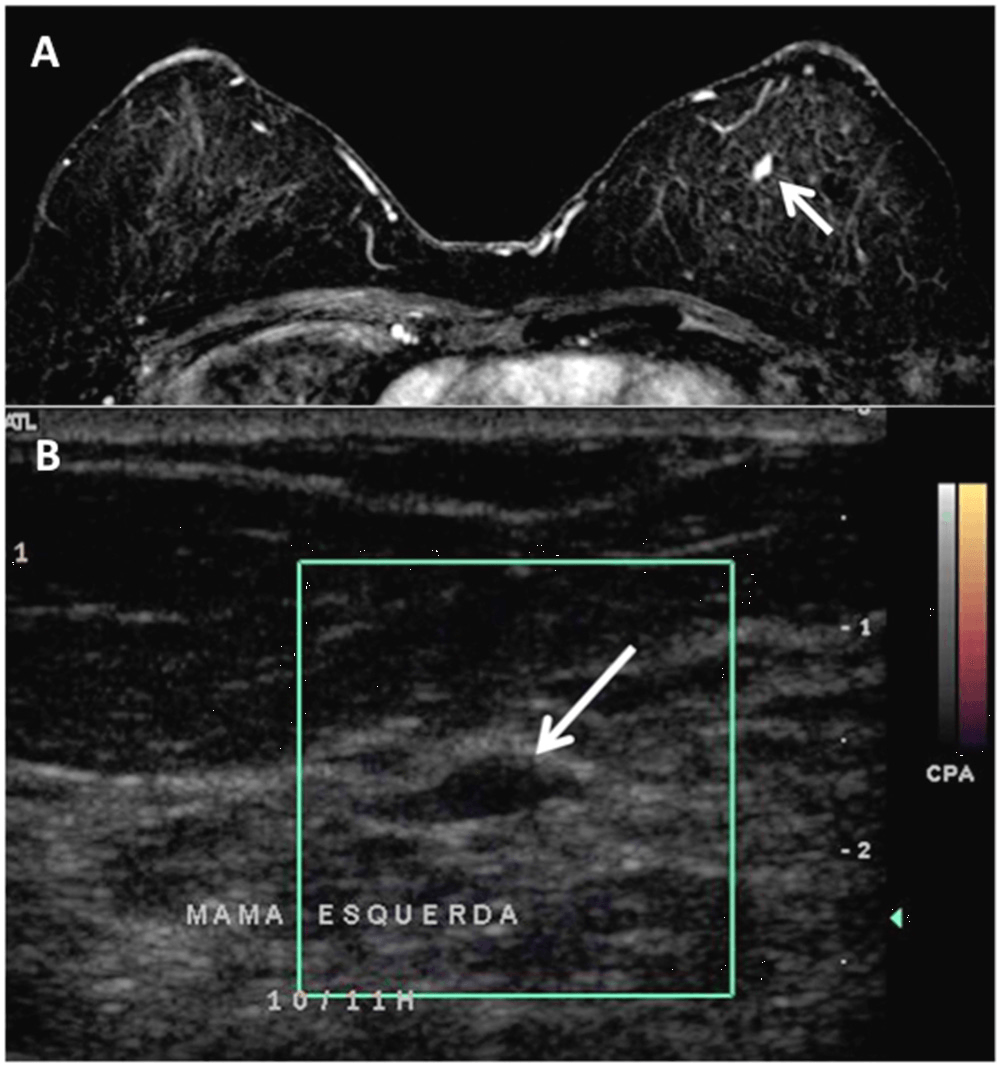
Наблюдалась прямая связь (p=0,025) между УЗИ данными и BI–RADS-МРТ терминологией (Таблица 2). На Рис. 1 изображен случай, в котором изменение очага BI–RADS 4 категории было обнаружено на МРТ молочной железы с прямой УЗИ корреляцией. Прямая связь между BI–RADS классификацией на МРТ и УЗИ (p<0,001) найдена во всех категориях (Таблица 3).
Гистологический анализ очагов классифицированных по шкале BI–RADS как категория 4 и 5 (n=22) показал, что 17 (77,3%) из них – доброкачественные очаги, а 5 (22,7%) – злокачественные (Таблица 4).
Таблица 2
Корреляция BI–RADS классификации на МРТ и результатов прицельного УЗИ (n=68).
|
BI–RADS-МРТ |
При цельное УЗИ |
В общем |
|
| Отрицательное | Положительное | ||
| категория 3 |
20 (43,6%) |
26(56,4%) |
46 (100%) |
| категория 4 |
2 (10%) |
18(90%) |
20 (100%) |
| категория 5 |
0 |
2(100%) |
2 (100%) |
p=0,025.
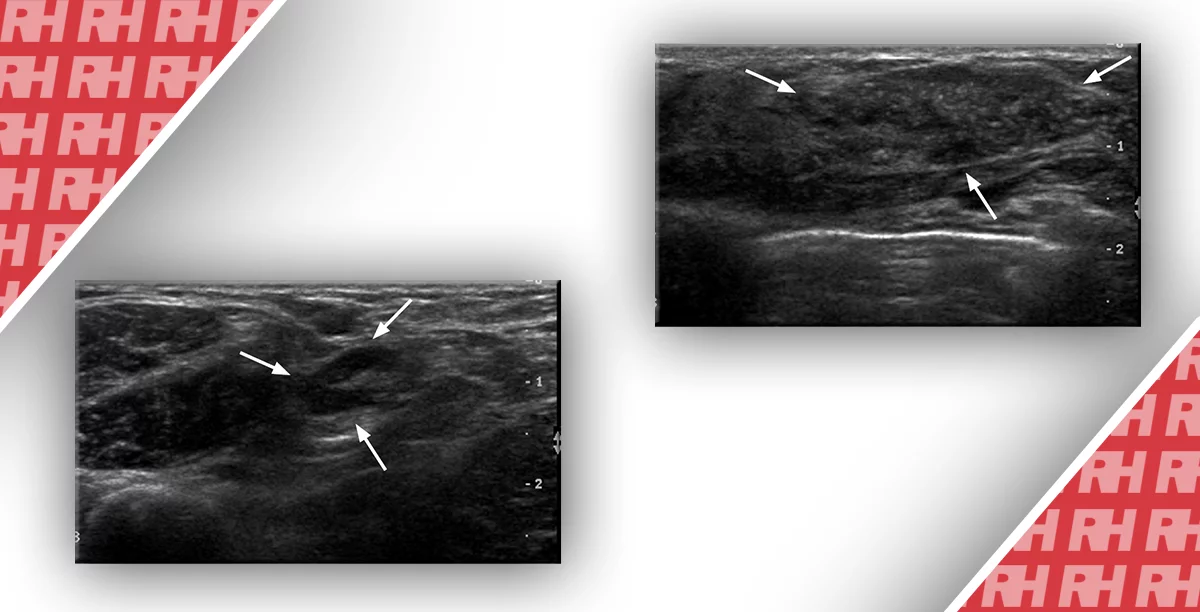
Рис. 1. МРТ снимки 52 летней женщины после правосторонней квадрантэктомии и радиотерапии (рак молочной железы). (А) Аксиальное Т1-взвешенное изображение с контрастным усилением, на котором видно овальное объемное образование (стрелка) с гладкими контурами, гомогенным контрастным усилением, и кинетической кривой II типа (BI–RADS 4) в верхнемедиальном квадранте левой молочной железы. (В) Прицельное УЗИ показало интрадуктальное овальное объемное образование (стрелка), горизонтальное, ограниченное, и гипоэхогенное в верхнемедиальном квадранте левой молочной железы, которое не было обнаружено при первом УЗИ. При помощи пункционной биопсии под контролем УЗ обнаружено интрадуктальную папиллому.
Таблица 3
Корреляция BI–RADS классификации при МРТ и УЗИ патологических очагов, найденных на прицельном УЗИ (n=46).
| BI–RADS-МРТ |
BI–RADS-УЗИ |
В общем |
||
|
категория 3 |
категория 4 |
категория 5 |
||
| категория 3 |
24 (92.3%) |
2 (6.7%) |
0 |
26 (100%) |
| категория 4 |
3 (16.7%) |
14 (77.8%) |
1 (5.5%) |
18 (100%) |
| категория 5 |
0 |
0 |
2 (100%) |
2 (100%) |
p<0.001.
Два очага BI–RADS 4 категории, которые не нашли на прицельном УЗИ, подлежали хирургической биопсии после предоперационной маркировки гарпуном под контролем МРТ (ROLL– RadioguidedOccultLesionLocalization), и обе были доброкачественными. Девять очагов BIRADS 3 категории найдены на прицельном УЗИ подлежали перкутанной биопсии и все были доброкачественными. Ни один из очагов BIRADS 3 категории, обнаруженый на МРТ, но не найден при прицельном УЗИ, не изменился в размере или форме на протяжении периода наблюдения.
Таблица 4
Корреляция BI–RADS классификации при магнитно-резонансной томографии (МРТ) и гистологическом исследовании (n=31).
|
BI–RADS-МРТ |
Гистология |
В общем |
|
|
Доброкачественные образования |
Злокачественные образования |
||
|
категория 3 |
9 (100%) |
– |
9 (100%) |
|
категория 4 |
16 (80%) |
4 (20%) |
20 (100%) |
|
категория 5 |
1 (50%) |
1 (50%) |
2 (100%) |
p=0,025.
ОБСУЖДЕНИЕ
Предыдущие работы сообщали о вероятности идентификации на повторном прицельном УЗИ патологических очагов найдены на МРТ (19-89%). Такой большой разброс объясняется тем, что использовались разные методы (ретроспективные работы, отсутствие установленных критериев показаний на обследование, отсутствие УЗИ данных до МРТ исследования, т.д.).. В данной работе, при помощи прицельного УЗИ обнаружено 67,6% патологических очагов найдены на МРТ, но ранее не диагностированных при помощи других методов (все BI-RADS категории 5, большинство BI-RADS категории 4, и примерно половину BI-RADS категории 3). Эти данные доказывают, что с помощью УЗИ можно эффективно идентифицировать подозрительные злокачественные очаги.
Способность ультразвука обнаруживать ранее не диагностированные патологические очаги не имело прямой связи с размерами и характеристиками очагов найдены на МРТ. Однако, предыдущие работы показали, что вероятность идентификации патологического очага найденного на МРТ используя прицельное УЗИ прямо пропорционально к его размеру и варьирует в зависимости от типа очага (выше для объемных образований чем для фокальных или необъемных патологических очагов). Данные прицельного УЗИ могут быть атипическими и неубедительными.
В данной работе, мы решили включить подозрительные очаги (BI–RADS категории 4 и 5) и те которые наверняка были доброкачественными (BI–RADS категории 3). Прицельное УЗИ помогает охарактеризовать подозрительный очаг, сделать перкутанную биопсию под УЗ контролем, и является дешевым, быстрым, более доступным, и комфортным методом для пациента. Но, если отсутствует корреляция при прицельном УЗИ, стоит сделать биопсию подозрительных очагов под контролем МРТ или стереотаксический метод. Для доброкачественных очагов, найденных на МРТ, сфокусированное повторное УЗИ дает возможность охарактеризовать очаг, и проводить последующее наблюдение (учитывая недостатки МРТ для мониторинга таких очагов). Кроме того, вероятность малигнизации очага, найденного при помощи МРТ, возрастает, если есть корреляция при прицельном УЗИ.
В нашем исследовании повторное УЗИ сумело идентифицировать все злокачественные очаги. Небольшое количество злокачественных очагов в нашей работе объясняется обязательным проведением МРТ пациентам, у которых были неубедительные заключения маммографических или ультразвуковых исследований и скрининга. В литературе, вероятность обнаружения ракового процесса при сфокусированном УЗИ колеблется от 8% до 56%, со средним взвешенным числом 36%.
УЗИ свойственны некоторые характеристики, такие как оператор-зависимость, что предусматривает специфическую подготовку оператора для оценки тканей молочной железы. Было высказано предложение, что если один и тот же радиолог выполнял прицельное УЗИ и МРТ, результаты будут более точными. Тем не менее, Boschetal. показали значительную степень согласованности между исследователями, если УЗИ молочной железы было выполнено ими при наличии необходимого объема знаний, не смотря на разницу в их опыте. В большинстве случаев, прицельное УЗИ выполняли два радиолога. Результаты нашей работы имеют высокую воспроизводимость при соблюдении следующих условий: исследование выполняется профессионалом с опытом в области визуализации молочной железы с использованием адекватной аппаратуры. Применение повторного УЗИ с объемной навигацией является новым альтернативным методом для объективного сравнения МРТ и УЗИ данных. Эта особенность дает значительно высшую вероятность обнаружения патологического очага, и уменьшает зависимость от оператора.
ВЫВОДЫ
Прицельное повторное (secondlook) УЗИ может определить большую часть патологических очагов найденных только при МРТ молочной железы, особенно очаги высокого риска малигнизации, в случае его проведения профессионалом с опытом в УЗИ и МРТ молочной железы.
Откройте для себя расширенные функциональные возможности с ультразвуковой диагностической системой Medison Accuvix XG. Только лучшие предложения от компании RH.










14.10.2019
Василий